题目内容
12.下面为CO2加氢制取乙醇的反应:2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g)
△H=QkJ/mol (Q>0)
在密闭容器中,按CO2与H2的物质的量之比为1:3进行投料,在5MPa下测得不同温度下平衡体系中各种物质的体积分数(y%)如图1所示.完成下列填空:
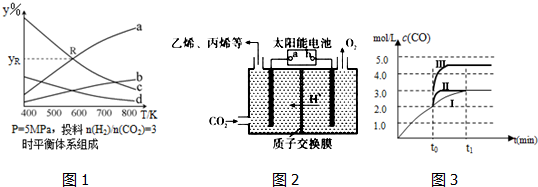
(1)表示CH3CH2OH体积分数曲线的是b(选填序号).
(2)图1中曲线a和c的交点R对应物质的体积分数 yR=37.5%.
(3)在强酸性的电解质水溶液中,惰性材料做电极,电解CO2可得到多种燃料,其原理如图2所示.
①该工艺中能量转化方式主要有太阳能转化为电能,电能转化为化学能.
②电解时,生成乙烯的电极反应式2CO2+12H++12e-=C2H4+4H2O.
(4)在3L容积可变的密闭容器中发生反应,H2(g)+CO2(g)?H2O (g)+CO(g)已知c(CO)-反应时间t变化曲线Ⅰ如图3所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ.当曲线Ⅰ变为曲线Ⅱ时,改变的条件是加入催化剂.
当曲线Ⅰ变为曲线Ⅲ时,改变的条件是将容器的体积快速压缩至2L.
分析 (1)该反应为吸热反应,升高温度平衡正向移动,平衡时CO2与H2的含量降低,CH3CH2OH与H2O的含量增大.开始CO2 与H2 的物质的量之比1:3进行,平衡时H2的含量是CO2的含量三倍;CH3CH2OH与H2O按1:3生成,平衡时H2O的含量是CH3CH2OH含量的三倍;
(2)R点为a和c的交点,设此时a的H2O体积为V,那么c的H2体积也为V,根据方程式中的关系求出CO2和CH3CH2OH的体积,再求体积分数ya;
(3)太阳能电池为电源,电解强酸性的二氧化碳水溶液得到乙烯,乙烯在阴极生成.据此解答;
(4)图象分析曲线Ⅰ变化为曲线Ⅱ是缩短反应达到平衡的时间,最后达到相同平衡状态,体积是可变得是恒压容器,说明改变的是加入了催化剂;当曲线Ⅰ变为曲线Ⅲ时一氧化碳物质的量增大,反应是气体体积不变的反应,可变容器中气体体积和浓度成反比,气体物质的量不变.
解答 解:(1)该反应为吸热反应,升高温度平衡正向移动,平衡时CO2与H2的含量降低,CH3CH2OH与H2O的含量增大.开始CO2 与H2 的物质的量之比1:3进行,平衡时H2的含量是CO2的含量三倍;CH3CH2OH与H2O按1:3生成,平衡时H2O的含量是CH3CH2OH含量的三倍;
曲线a、曲线b随温度升高含量增大,且曲线a的含量高,所以曲线a表示H2O、曲线b表示CH3CH2OH;
曲线c、曲线d随温度升高含量减小,且曲线c的含量高,所以曲线c表示H2、曲线d表示CO2.
故答案为:b;
(2)2CO2(g)+6H2(g)=CH3CH2OH(g)+3H2O(g);
R点为a和c的交点,设此时a的H2O体积为6V,那么c的H2体积也为6V,根据方程式可知CO2为$\frac{6V}{6}$=2V,C2H5OH为$\frac{6V}{3}$=2V,
所以R点对应的体积分数ya=$\frac{6V}{6V+6V+2V+2V}$×100%=37.5%,
故答案为:37.5;
(3)①太阳能电池为电源,电解强酸性的二氧化碳水溶液得到乙烯,可知能量转化形式有光能转化为电能,电能转化为化学能,部分电能转化为热能,故答案为:太阳能转化为电能,电能转化为化学能;
②电解时,二氧化碳在b极上生成乙烯,得到电子的一极为电源的正极,电极反应式为2CO2+12H++12e-=C2H4+4H2O,故答案为:2CO2+12H++12e-=C2H4+4H2O;
(4)图象分析曲线Ⅰ变化为曲线Ⅱ是缩短反应达到平衡的时间,最后达到相同平衡状态,体积是可变得是恒压容器,说明改变的是加入了催化剂;当曲线Ⅰ变为曲线Ⅲ时一氧化碳物质的量增大,反应是气体体积不变的反应,可变容器中气体体积和浓度成反比,气体物质的量不变,曲线Ⅰ,体积为3L,一氧化碳浓度为3mol/L,改变条件不好为曲线Ⅱ,一氧化碳浓度为4.5mol/L,则体积压缩体积为:3:V=4.5:3,V=2L,所以将容器的体积快速压缩至2L符合;
故答案为:加入催化剂;将容器的体积快速压缩至2L.
点评 本题考查学生对图象的分析与平衡移动及平衡状态的特征的理解以及原电池反应等知识,难度较大,注意判断曲线表示哪一物质的体积分数是关键.

 乙醇分子中不同的化学键如图所示,对乙醇在各种反应中应断裂的键说明不正确的是( )
乙醇分子中不同的化学键如图所示,对乙醇在各种反应中应断裂的键说明不正确的是( )| A. | 与金属钠作用时,键①断 | |
| B. | 浓硫酸共热至170℃时,键②和⑤断裂 | |
| C. | 和乙酸、浓硫酸共热时,键②断裂 | |
| D. | 在银催化下和氧气反应时,键①和④断裂 |
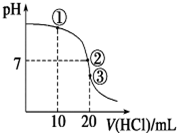 常温下,在20.00mL 0.100 0mol•L-1 NH3•H2O溶液中逐滴滴加0.1000mol•L-1 HCl溶液,溶液pH随滴入HCl溶液体积的变化曲线如右图所示.下列说法正确的是( )
常温下,在20.00mL 0.100 0mol•L-1 NH3•H2O溶液中逐滴滴加0.1000mol•L-1 HCl溶液,溶液pH随滴入HCl溶液体积的变化曲线如右图所示.下列说法正确的是( )| A. | ①溶液:c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| B. | ②溶液:c(NH4+)=c(Cl-)>c(OH-)=c(H+) | |
| C. | ①、②、③三点所示的溶液中水的电离程度②>③>① | |
| D. | 滴定过程中不可能出现:c(NH3•H2O)>c(NH4+)>c(OH-)>c(Cl-)>c(H+) |
①碘水、淀粉溶液 ②氯水、CCl4 ③溴水、苯 ④硝酸、AgNO3溶液 ⑤氯水、苯 ⑥氯水、盐酸.
| A. | ①②④ | B. | ②③⑥ | C. | ②④⑤ | D. | ④⑤⑥ |
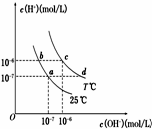 在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系.下列条件关于离子共存说法中正确的是( )
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系.下列条件关于离子共存说法中正确的是( )| A. | a点对应的溶液中大量存在:Fe3+、Ba2+、K+、NO3- | |
| B. | b点对应的溶液中大量存在:Na+、K+、NH4+、Cl- | |
| C. | d点对应的溶液中大量存在:Na+、Ba2+、Cl-、Al3+ | |
| D. | c点对应的溶液中大量存在:CO32-、Na+、Cu2+、SO42- |
| A. | O3和NO2 | B. | CH4和NH4+ | C. | N2O和CO2 | D. | PCl3和SO32- |
| A. | 1mol甲基中含有的电子数为10NA | |
| B. | 1mol乙醇中含有C-H键的数目为6NA | |
| C. | 300mL2mol/L乙醇水溶液中所含H原子数为3.6NA | |
| D. | 常温常压下,7.0g乙烯与丙烯的混合物中含有氢原子的数目为NA |
| A. | 电子由锌片流出 | |
| B. | 锌比铜活泼,所以锌作正极 | |
| C. | 溶液中c(H+)减小 | |
| D. | 当有6.5g锌溶解时电路中转移的电子数是0.2NA |
| A. | 新制氯水只含有氯分子和次氯酸两种分子 | |
| B. | 氯水放置数天后,其酸性逐渐减弱 | |
| C. | 氯水光照时有气泡逸出,该气体的主要成分是氯气 | |
| D. | 向Na2O与水反应后的溶液中通入适量氯气后,溶液中含有两种溶质 |