题目内容
7.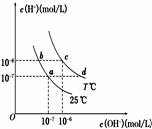 在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系.下列条件关于离子共存说法中正确的是( )
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系.下列条件关于离子共存说法中正确的是( )| A. | a点对应的溶液中大量存在:Fe3+、Ba2+、K+、NO3- | |
| B. | b点对应的溶液中大量存在:Na+、K+、NH4+、Cl- | |
| C. | d点对应的溶液中大量存在:Na+、Ba2+、Cl-、Al3+ | |
| D. | c点对应的溶液中大量存在:CO32-、Na+、Cu2+、SO42- |
分析 水的离子积为Kw=c(H+)×c(OH-),由图可知,a、b均在25℃,离子积相同;而c、d均在T℃,离子积相同,并结合离子之间不发生化学反应来解答.
解答 解:A.Fe3+水解显酸性,而a点对应的溶液显中性,则离子不能大量共存,故A错误;
B.b点c(H+)>c(OH-),溶液显酸性,该组离子之间不反应,能大量共存,故B正确;
C.d点c(H+)<c(OH-),对应的溶液显碱性,Al3+不能大量存在,故C错误;
D.c点时c(H+)=c(OH-),溶液为中性,CO32-水解显碱性,且CO32-、Cu2+结合生成沉淀,不能大量共存,故D错误;
故选B.
点评 本题考查离子的共存,为高频考点,把握图象中各点对应的溶液的酸碱性是解答本题的关键,注意T℃>25℃为学生解答的难点,题目难度不大.

练习册系列答案
相关题目
12.下列离子方程式正确的是( )
| A. | 草酸可使酸性高锰酸钾溶液褪色,其离子方程式为:2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O | |
| B. | 向NH4Al(SO4)2溶液中加入过量的Ba(OH)2稀溶液:NH4++Al3++2SO42-+2Ba2++5OH-=2BaSO4↓+NH3•H2O+AlO2-+2H2O | |
| C. | NaHSO3溶液与FeCl3反应的离子方程式:SO32-+2Fe3++H2O=SO42-+2Fe2++2H+ | |
| D. | NH4HCO3溶液中加入少量NaOH:NH4++OH-═NH3•H2O |
13.下列说法正确的是( )
| A. | 乙烯使溴水或酸性高锰酸钾溶液褪色均属于加成反应 | |
| B. | 常温常压下环癸五烯 是一种易溶于水的无色气体 是一种易溶于水的无色气体 | |
| C. | 用酸性重铬酸钾溶液检验酒驾,发生的反应属于乙醇的氧化反应 | |
| D. | 等质量的乙烯和乙醇完全燃烧,消耗O2的物质的量相同 |
2.下列关于σ键和π键的理解不正确的是( )
| A. | 共价单键都是σ键,共价双键中有一个σ键和一个π键 | |
| B. | σ键可以绕键轴旋转,π键一定不能绕键轴旋转 | |
| C. | HBr 分子中的σ键是s-p σ键,Cl2分子中的σ键是p-p σ键 | |
| D. | 气体单质中一定存在σ键,可能存在π键 |
16.下列事实不能用元素周期律解释的是( )
| A. | 相对原子质量:Ar>K | B. | 碱性:NaOH>Mg(OH)2 | ||
| C. | 酸性:HNO3>H3PO4 | D. | 元素非金属性:Cl>S |
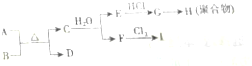
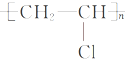 ;
;
 ,分子的立体构型是平面三角形.
,分子的立体构型是平面三角形. ,与CCl4互为等电子体的分子和离子分别有SiCl4和SO42-(各举一例,写化学式).
,与CCl4互为等电子体的分子和离子分别有SiCl4和SO42-(各举一例,写化学式).