题目内容
4.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )| A. | 1mol甲基中含有的电子数为10NA | |
| B. | 1mol乙醇中含有C-H键的数目为6NA | |
| C. | 300mL2mol/L乙醇水溶液中所含H原子数为3.6NA | |
| D. | 常温常压下,7.0g乙烯与丙烯的混合物中含有氢原子的数目为NA |
分析 A.甲基中含有9个电子,1mol甲基中含有9mol电子;
B.根据乙醇分子的结构计算出含有的碳氢键数目;
C.乙醇是非电解质不电离,溶液中水中也含有氢原子;
D.乙烯与丙烯的最简式相同为CH2,根据n=$\frac{m}{M}$计算最简式的物质的量,H原子物质的量是最简式的2倍,再根据N=nNA计算.
解答 解:A.甲基甲烷少1个电子,1mol甲基中含有9mol电子,含有的电子数为9NA,故A错误;
B.1mol乙醇分子中含有5mol碳氢键,含有C-H键的数目为5NA,故B错误;
C.乙醇是非电解质不电离,溶液中水中也含有氢原子,300mL 2mol/L乙醇水溶液中所含H原子数大于3.6NA,故C错误;
D.乙烯与丙烯的最简式相同为CH2,最简式的物质的量为$\frac{7g}{14g/mol}$=0.5mol,故H原子物质的量为1mol,含有H原子数目为NA,故D正确;
故选:D.
点评 本题考查了阿伏伽德罗常数的分析应用,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系是解题关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.下表所示的五种元素中,W、X、Y、Z为短周期元素,X元素的单质是空气中含量最多的成分.下列说法正确的是( )
| X | Y | ||
| W | Z | ||
| T |
| A. | X位于元素周期表中第二周期ⅤA族 | |
| B. | Y、Z形成氢化物的沸点更高是Z | |
| C. | 由X、Y和氢三种元素形成的化合物中只有共价键 | |
| D. | 元素T与X的原子序数相差25 |
16.下列事实不能用元素周期律解释的是( )
| A. | 相对原子质量:Ar>K | B. | 碱性:NaOH>Mg(OH)2 | ||
| C. | 酸性:HNO3>H3PO4 | D. | 元素非金属性:Cl>S |
13.可逆反应A(g)+3B(g)?2C(g)+2D(g)在4种不同情况下反应速率分别如下,其中反应速率最大的是( )
| A. | v(A)=0.15mol/(L•min) | B. | v(B)=0.3 mol/(L•min) | ||
| C. | v(C)=0.2 mol/(L•min) | D. | v(D)=0.1 mol/(L•min) |
14.在实验室进行下列实验,括号内的实验仪器、试剂都能用到的是( )
| A. | 乙炔的制备(蒸馏烧瓶、温度计、分液漏斗) | |
| B. | 蛋白质的盐析(试管、醋酸铅溶液、鸡蛋清溶液) | |
| C. | 蔗糖的水解(试管、蔗糖溶液、稀硫酸) | |
| D. | 肥皂的制取(蒸发皿、玻璃棒、甘油) |
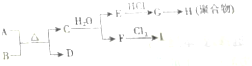
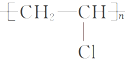 ;
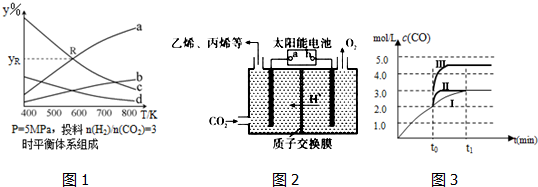
;
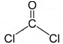 ,分子的立体构型是平面三角形.
,分子的立体构型是平面三角形.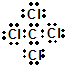 ,与CCl4互为等电子体的分子和离子分别有SiCl4和SO42-(各举一例,写化学式).
,与CCl4互为等电子体的分子和离子分别有SiCl4和SO42-(各举一例,写化学式).
 ;
;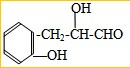 或
或 .
.