题目内容
17.下列各组粒子不属于等电子体的是( )| A. | O3和NO2 | B. | CH4和NH4+ | C. | N2O和CO2 | D. | PCl3和SO32- |
分析 电子数目相同的微粒为等电子体,原子数相同,电子总数相同的分子,互称为等电子体,原子数总数相同、价电子总数相同的分子,也互称为等电子体,分子中质子数=电子数,阳离子电子数=质子数-所带电荷数,阴离子电子数=质子数+所带电荷数,据此结合选项判断.
解答 解:A.O3和NO2原子数总数相同,O3的质子数为8×3=24,NO2的质子数为7+8×2=23,分子中质子数=电子数,所以两者的电子数不相等,价电子数分别为6×3=18、5+6×2=17不相等,所以不属于等电子体,故A正确;
B.CH4和NH4+原子数总数相同,CH4的质子数为6+4×1=10,NH4+的质子数为7+4×1=11,分子中质子数=电子数,阳离子电子数=质子数-所带电荷数,CH4的电子数为10,NH4+的电子数为10,所以两者的电子数,相等,是等电子体,故B错误;
C.N2O和CO2原子数总数相同,N2O的质子数为7×2+8=22,CO2的质子数为6+8×2=22,分子中质子数=电子数,所以两者的电子数相等,属于等电子体,故C错误;
D.PCl3和SO32-原子数总数相同,PCl3的价电子总数为5+7×3=26,SO32-的价电子总数为6+6×3+2=26,所以两者的价电子数相等,属于等电子体,故D错误;
故选A.
点评 本题考查了等电子体的含义,解答本题的关键是要充分理解等电子体的本质特征,题目难度不大.

练习册系列答案
相关题目
3.现有7瓶失去了标签的液体,已知它们是有机溶剂,可能是①乙醇②乙酸 ③苯④乙酸乙酯 ⑤油脂⑥葡萄糖⑦蔗糖溶液,现通过如下实验步骤来确定试剂中所装的液体名称.
(1)试给它们的试剂瓶重新贴上标签:
A乙醇、B乙酸、C苯、D乙酸乙酯、E油脂、F葡萄糖溶液、G蔗糖溶液;
(2)写出在D中加入NaOH溶液并加热的化学方程式.CH3COOCH2CH3+NaOH$\stackrel{△}{→}$CH3COONa+CH3CH2OH
(3)已知乙醛发生银镜反应的化学方程式为:
CH3CHO+4[Ag(NH3)2]OH $\stackrel{△}{→}$ (NH4)2CO3+4Ag↓+6NH3↑+2H2O.
试写出葡萄糖发生银镜反应的化学方程式为CH2OH(CHOH)4CHO+2Ag(NH3)2OH$\stackrel{△}{→}$H2O+2Ag↓+3NH3+CH2OH(CHOH)4COONH4.
| 实验步骤和方法 | 实验现象 |
| ①把7瓶液体分别依次标号A、B、C、D、E、F、G后闻气味 | 只有F、G两种液体没有气味 |
| ②各取少量于试管中加水稀释 | 只有C、D、E三种液体不溶解而浮在水上层 |
| 分别取少量7种液体于试管中加新制的Cu(OH)2并加热 | 只有B使沉淀溶解,F中产生红色沉淀 |
| 各取C、D、E少量于试管中,加稀NaOH溶液并加热 | 只有C仍有分层现象,且在D的试管中闻到特殊香味 |
A乙醇、B乙酸、C苯、D乙酸乙酯、E油脂、F葡萄糖溶液、G蔗糖溶液;
(2)写出在D中加入NaOH溶液并加热的化学方程式.CH3COOCH2CH3+NaOH$\stackrel{△}{→}$CH3COONa+CH3CH2OH
(3)已知乙醛发生银镜反应的化学方程式为:
CH3CHO+4[Ag(NH3)2]OH $\stackrel{△}{→}$ (NH4)2CO3+4Ag↓+6NH3↑+2H2O.
试写出葡萄糖发生银镜反应的化学方程式为CH2OH(CHOH)4CHO+2Ag(NH3)2OH$\stackrel{△}{→}$H2O+2Ag↓+3NH3+CH2OH(CHOH)4COONH4.
2.短周期元素形成的离子X2-与Y+都与Ne原子具有相同的电子层结构,则下列叙述中正确的是( )
| A. | 原子序数X>Y | B. | 原子半径X<Y | ||
| C. | X和Y一定同周期 | D. | X是第ⅡA族元素,Y是第VⅡA族元素 |
6.已知分子式为C10H14的有机物,该有机物不能与溴水发生加成反应,分子中只有一个烷基,此烷基的结构有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
7.下列反应的离子方程式书写不正确的是( )
| A. | 钠和冷水反应:2Na+2H2O=2Na++2OH-+H2↑ | |
| B. | 氧化亚铁溶于盐酸:FeO+2H+=Fe2++H2O | |
| C. | FeCl2溶液与Cl2反应:2Fe2++Cl2=2Fe3++2Cl- | |
| D. | 碳酸钠溶液与石灰乳的反应:CO32-+Ca2+=CaCO3↓ |
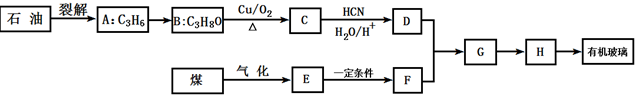
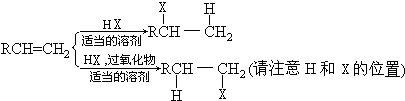
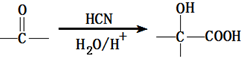
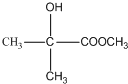 ;有机玻璃的链节是:
;有机玻璃的链节是: ;
;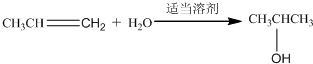 ;
;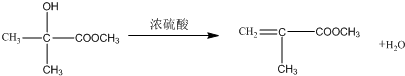 .
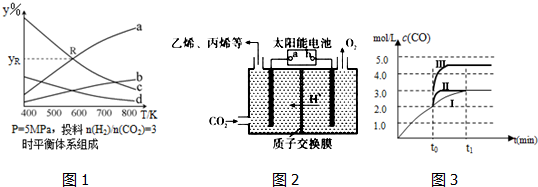
.

 ;
;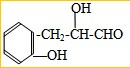 或
或 .
.