题目内容
12.下列叙述正确的是( )| A. | 蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有性脱水性 | |
| B. | 硫粉在过量的氧气中燃烧可以生成SO3 | |
| C. | 将SO2通入BaCl2溶液能生成白色沉淀 | |
| D. | 可用澄清石灰水溶液鉴别 CO2和SO2 |
分析 A.浓硫酸的脱水性是分子中氢和氧按2:1易水的形式脱去;
B.不符合反应客观事实;
C.亚硫酸酸性弱于盐酸,依据强酸制备弱酸规律解答;
D.SO2和CO2气体都可使澄清石灰水变浑浊,无法鉴别.
解答 解:A.浓硫酸可将许多有机化合物反应时,按水分子中氢、氧原子数的比(2:1)夺取这些有机物分子里的氢原子和氧原子,在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性,故A正确;
B.硫粉在过量的氧气中燃烧生成二氧化硫,故B错误;
C.亚硫酸酸性弱于盐酸,依据强酸制备弱酸规律,二氧化硫通入氯化钡溶液不会发生反应,故C错误;
D.SO2和CO2气体都可使澄清石灰水变浑浊,无法鉴别,故D错误;
故选:A.
点评 本题考查了元素化合物知识,侧重考查二氧化硫、浓硫酸,熟悉二种物质的性质是解题关键,注意浓硫酸吸水性、脱水性区别,题目难度不大.

练习册系列答案
相关题目
3.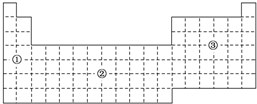 如果把元素周期表分为下面3个区域,则最活泼的金属、最活泼的非金属、最不活泼的非金属元素分别位于( )
如果把元素周期表分为下面3个区域,则最活泼的金属、最活泼的非金属、最不活泼的非金属元素分别位于( )
 如果把元素周期表分为下面3个区域,则最活泼的金属、最活泼的非金属、最不活泼的非金属元素分别位于( )
如果把元素周期表分为下面3个区域,则最活泼的金属、最活泼的非金属、最不活泼的非金属元素分别位于( )| A. | ①区、③区、③区 | B. | ①区、③区、②区 | C. | ①区、②区、②区 | D. | ②区、③区、③区 |
20.以下物质:(1)甲烷;(2)苯;(3)聚乙烯;(4)乙醇;(5)乙炔;(6)一氯乙烯; (7)甲苯;(8)苯乙烯(C6H5-CH=CH2).既能使KMnO4酸性溶液褪色,又能使溴水因发生化学反应而褪色的是( )
| A. | (3)(5)(8) | B. | (5)(6)(8) | C. | (5)(7)(8) | D. | (3)(5)(7)(8) |
7.将元素周期表原先的主、副族族号取消,从左往右改为18列,碱金属为第1列,稀有气体为第18列,按这个规定,下列说法不正确的是( )
| A. | 不仅有第2列元素的原子最外层有2个电子 | |
| B. | 第3~12列元素全为金属 | |
| C. | 第3列元素种类最多 | |
| D. | 第15、16、17列元素都是非金属元素 |
17.历史上最早应用的还原性染料是靛蓝,其结构简式如下图.下列关于靛蓝的叙述中错误的是( ) 

| A. | 靛蓝由碳、氢、氧、氮四种元素组成 | B. | 它的分子式是C16H10N2O2 | ||
| C. | 该物质不属于烃 | D. | 它是不饱和烃 |
7.二氧化碳和钠在一定条件下反应可制得金刚石,其化学方程式为3CO2+4Na=2X+C(金刚石).下列有关此反应的叙述中,不正确的是( )
| A. | Na通常保存在煤油中,而同族的Li只能保存在液体石蜡中 | |
| B. | 金刚石与石墨互为同素异形体,已知 燃烧热金刚石更高,则石墨比金刚石更稳定 | |
| C. | X的化学式为Na2CO3,若Mg 与CO2则生成MgO和C | |
| D. | 当有0.4molNa参与反应时,被氧化的CO2为0.3NA |
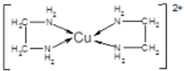
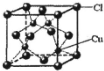 ,其中Cl-的配位数为4,已知晶胞的棱长为dcm,用NA表示阿伏加德罗常数值,则晶胞的密度表达式为$\frac{396}{{d}^{3}•{N}_{A}}$g/cm3.
,其中Cl-的配位数为4,已知晶胞的棱长为dcm,用NA表示阿伏加德罗常数值,则晶胞的密度表达式为$\frac{396}{{d}^{3}•{N}_{A}}$g/cm3.