题目内容
4.ALAl2(SO4)3溶液中,含有B mol Al3+,则此盐溶液中溶质的物质的量浓度为( )| A. | $\frac{B}{A}$ mol•L-1 | B. | $\frac{2A}{B}$mol•L-1 | C. | $\frac{A}{2B}$mol•L-1 | D. | $\frac{B}{2A}$mol•L-1 |
分析 根据硫酸铝的化学式及铝离子的物质的量计算出硫酸铝的物质的量,再根据c=$\frac{n}{V}$计算出该硫酸铝溶液的物质的量浓度.
解答 解:AL Al2(SO4)3溶液中含有B mol Al3+,则该溶液中含有硫酸铝的物质的量为Bmol×$\frac{1}{2}$=0.5Bmol,
该溶液中硫酸铝的物质的量浓度为$\frac{0.5Bmol}{AL}$=$\frac{B}{2A}$mol/L,
故选D.
点评 本题考查了物质的量浓度的计算,题目难度中等,明确物质的量浓度的概念及表达式为解答关键,注意掌握溶质化学式与含有离子的物质的量关系计算方法,试题培养了学生的化学计算能力.

练习册系列答案
相关题目
14.下列能说明HA是弱酸的是( )
①取0.01mol/LHA溶液测其pH大于2
②将pH等于2的HA溶液稀释100倍,pH等于4
③向pH等于4的HA溶液中加入少量NaA固体,pH变为5
④将pH等于4的HA溶液升高温度,pH基本不变
⑤HA溶液的导电性比HCI弱
⑥等pH值等体积的HA和盐酸溶液与足量的锌粒反应,盐酸放出的氢气少.
①取0.01mol/LHA溶液测其pH大于2
②将pH等于2的HA溶液稀释100倍,pH等于4
③向pH等于4的HA溶液中加入少量NaA固体,pH变为5
④将pH等于4的HA溶液升高温度,pH基本不变
⑤HA溶液的导电性比HCI弱
⑥等pH值等体积的HA和盐酸溶液与足量的锌粒反应,盐酸放出的氢气少.
| A. | ①③⑤ | B. | ②③⑥ | C. | ①③⑥ | D. | ①⑤⑥ |
12.下列各组物质在溶液中起反应时,离子方程式相同的是( )
| A. | 氯化钡与硫酸钠,氢氧化钡与硫酸 | |
| B. | 碘化钾与氯气,溴化钾与氯气 | |
| C. | 碳酸银与盐酸,硝酸银与盐酸 | |
| D. | 碳酸氢钠与稀硫酸,碳酸氢钾与盐酸 |
19.t℃时,CuSO4在水中的溶解度为25g,将32gCuSO4白色粉末加入mg水中形成饱和CuSO4溶液并有CuSO4•5H2O晶体析出,则m的取值范围是( )
| A. | 18g≤m≤128g | B. | 36g<m<180g | C. | 18g<m<128g | D. | 36g≤m≤180g |
9.下列关于仪器的识别中错误的是( )
| A. |  分液漏斗 | B. |  蒸发皿 | C. |  坩埚钳 | D. |  滴瓶 |
16.关于分类的知识说法错误的是( )
| A. | 分类法是学习和研究化学物质及化学变化的一种科学方法 | |
| B. | 常见的分类方法有交叉分类法和树形分类法 | |
| C. | 对于相同的分类对象,采用的分类标准不同,分类的结果也不同 | |
| D. | 初中的化学知识告诉我们,化学反应可以分为化合反应和分解反应两大类 |
13.向含有1molKAl(SO4)2的溶液中逐滴加入氢氧化钡溶液,充分反应.下列说法不正确的是( )
| A. | 当Al3+恰好完全沉淀时,消耗氢氧化钡1.5mol | |
| B. | 当SO42-恰好完全沉淀时,Al3+全部转化为Al(OH)3 | |
| C. | 当向溶液中加入1.5mol氢氧化钡时,反应可用下列离子方程式表示:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ | |
| D. | 反应过程中随加入的氢氧化钡的物质的量不断增大,沉淀的质量不断增大 |

 .
. .
.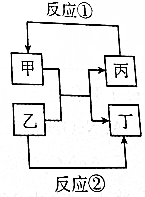 甲、乙、丙、丁四种取值的相互转化关系如图所示(部分反应物、产物及反应条件已略去).已知甲为常见金属(Na、Mg、Al、Fe、Cu)或其氧化物,回答下列问题:
甲、乙、丙、丁四种取值的相互转化关系如图所示(部分反应物、产物及反应条件已略去).已知甲为常见金属(Na、Mg、Al、Fe、Cu)或其氧化物,回答下列问题: