��Ŀ����
14��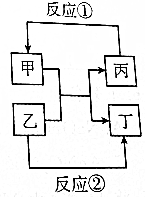 �ס��ҡ�����������ȡֵ���ת����ϵ��ͼ��ʾ�����ַ�Ӧ����P��Ӧ��������ȥ������֪��Ϊ����������Na��Mg��Al��Fe��Cu������������ش��������⣺
�ס��ҡ�����������ȡֵ���ת����ϵ��ͼ��ʾ�����ַ�Ӧ����P��Ӧ��������ȥ������֪��Ϊ����������Na��Mg��Al��Fe��Cu������������ش��������⣺��1������ΪFe3O4����ΪAl2O3 ����Ӧ�١���Ӧ������������ͬ������ΪAl���ѧʽ������Ӧ�ٵĻ�ѧ����ʽΪ3Fe+2O2��g��$\frac{\underline{\;��ȼ\;}}{\;}$Fe3O4��
��2������Ϊ�������ʣ���Ϊ��ɫ��������+�ҡ���+�������ӷ���ʽΪ2Na+2H2O+Cu2+=2Na++Cu��OH��2��+H2����
���� ��1������ΪFe3O4����ΪAl2O3 ����Ӧ�١���Ӧ������������ͬ�����ΪFe����Ӧ��Ϊ3Fe+2O2��g��$\frac{\underline{\;��ȼ\;}}{\;}$Fe3O4����ΪAl����������Ϊ������
��2����Ϊ�������ʣ���Ϊ��ɫ��������ΪCu��OH��2�����ΪNa����Ϊ��ͭ���ӵ�����Һ���Դ������
��� �⣺��1������ΪFe3O4����ΪAl2O3 ����Ӧ�١���Ӧ������������ͬ����������Ϊ���������ΪFe����Ӧ��Ϊ3Fe+2O2��g��$\frac{\underline{\;��ȼ\;}}{\;}$Fe3O4����ΪAl��
�ʴ�Ϊ��Al��
��2����Ϊ�������ʣ���Ϊ��ɫ��������ΪCu��OH��2�����ΪNa����Ϊ��ͭ���ӵ�����Һ�����+�ҡ���+�������ӷ���ʽΪ2Na+2H2O+Cu2+=2Na++Cu��OH��2��+H2����
�ʴ�Ϊ��2Na+2H2O+Cu2+=2Na++Cu��OH��2��+H2����
���� ���⿼��������ƶϣ�Ϊ��Ƶ���㣬���ճ������ʵ����ʼ��ת��Ϊ���Ĺؼ������ؽ��������û���Ӧ�������仯����ת���������仯����ת���Ŀ��飬�ۺ��Խ�ǿ����Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ
4��ALAl2��SO4��3��Һ�У�����B mol Al3+���������Һ�����ʵ����ʵ���Ũ��Ϊ��������
| A�� | $\frac{B}{A}$ mol•L-1 | B�� | $\frac{2A}{B}$mol•L-1 | C�� | $\frac{A}{2B}$mol•L-1 | D�� | $\frac{B}{2A}$mol•L-1 |
5��ijУ��ѧ����С��ͬѧ��װ�����������������������ӣ��Ʊ���ѧ��ѧ�ļ��ֳ������壮
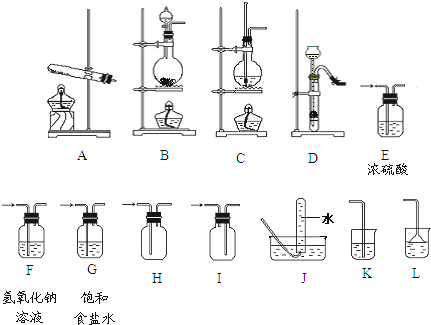
����д���б����еĿհ״���

����д���б����еĿհ״���
| ��� | ���� | װ�õ�����˳���÷��ű�ʾ�� | ��Ҫ�����Լ� ���� | ʵ������ȡ������ �ķ�Ӧ����ʽ �������ӷ�Ӧ��д���ӷ�Ӧ����ʽ�� |
| ��1�� | CO2 | �Ʊ����ռ� | ||
| ��2�� | NH3 | �Ʊ����ռ� ��β������ | �����������ѡ�õ��Լ� ��ʯ�� | |
| ��3�� | Cl2 | �Ʊ���������������ռ���β������ | ����β�� ���Լ� ����������Һ | |
| ��4�� | �Ʊ����������ռ� C��F��J |
9��������Һ���й��������ʵ���Ũ�ȹ�ϵ��ȷ���ǣ�������
| A�� | ͬŨ�ȵ�������Һ����NH4Al��SO4��2����NH4Cl����NH3•H2O����CH3COONH4������c��NH4+���ɴ�С��˳���ǣ��٣��ڣ��ۣ��� | |
| B�� | ��ͬ�¶��£��������Ȼ�������ֱ������ͬ�����Ģ�����ˮ����0.1mol•L-1���ᡢ��0.1mol•L-1�Ȼ�þ��Һ����0.1mol•L-1��������Һ�У�Ag+Ũ�ȣ��٣���=�ڣ��� | |
| C�� | �����½�NaHSO3��NaHCO3����Һ ��Ϻ���Һ�����ԣ����Ϻ����Һ�У�c��Na+��=c��HSO3-��+c��HCO3-��+2c��CO32-��+2c��SO32-�� | |
| D�� | ��ͬ�����£�pH=5�Ģ�NH4Cl��Һ����CH3COOH��Һ����ϡ����������Һ����ˮ�������c��H+�����٣��ڣ��� |
2�� ��ס��ҡ��������ܱ������г���һ������A��B��������Ӧ��A��g��+xB��g��?2C��g�����������ķ�Ӧ�¶ȡ���Ӧ����ʼ������Ӧ������C��Ũ����ʱ��仯��ϵ�ֱ��������ͼ��ʾ�������й��ƶ���ȷ���ǣ�������
��ס��ҡ��������ܱ������г���һ������A��B��������Ӧ��A��g��+xB��g��?2C��g�����������ķ�Ӧ�¶ȡ���Ӧ����ʼ������Ӧ������C��Ũ����ʱ��仯��ϵ�ֱ��������ͼ��ʾ�������й��ƶ���ȷ���ǣ�������
 ��ס��ҡ��������ܱ������г���һ������A��B��������Ӧ��A��g��+xB��g��?2C��g�����������ķ�Ӧ�¶ȡ���Ӧ����ʼ������Ӧ������C��Ũ����ʱ��仯��ϵ�ֱ��������ͼ��ʾ�������й��ƶ���ȷ���ǣ�������
��ס��ҡ��������ܱ������г���һ������A��B��������Ӧ��A��g��+xB��g��?2C��g�����������ķ�Ӧ�¶ȡ���Ӧ����ʼ������Ӧ������C��Ũ����ʱ��仯��ϵ�ֱ��������ͼ��ʾ�������й��ƶ���ȷ���ǣ������� | ���� | �� | �� | �� |
| �ݻ� | 0.5 L | 0.5 L | 1.0 L |
| �¶�/�� | T1 | T2 | T2 |
| ��Ӧ�� ��ʼ�� | 1.5 mol A 0.5 mol B | 1.5 mol A 0.5 mol B | 6.0 mol A 2.0 mol B |
| A�� | 10 min�ڼ������з�Ӧ��ƽ������v��A��=0.1 mol/��L•min�� | |
| B�� | T1��T2������ӦΪ���ȷ�Ӧ | |
| C�� | ƽ��ʱ�����¶Ȳ��䣬��С�������ƽ��������Ӧ�����ƶ� | |
| D�� | T1��ʱ������ʼʱ�������г���0.5 mol A��1.5 mol B��ƽ��ʱA��ת����Ϊ75% |
9��ˮú�� ����Ҫ�ɷ֣�CO��H2 �� ����Ҫȼ�Ϻͻ���ԭ�ϣ�����ˮ����ͨ�����ȵ�̿���Ƶã�
C ��s��+H2O��g��?CO ��g��+H2 ��g������H=+131.3kJ•mol-1
��1��ij�¶��£��ĸ������о�������������Ӧ����������̿�������������ʵ����ʵ���Ũ�ȼ����淴Ӧ���ʹ�ϵ���±���ʾ������д������Ӧ�Ŀո�
��2������һ���ݻ��ɱ���ܱ����������º�ѹ�£������м���1.0mol̿�� 1.0mo lˮ���� ��H216O��������������Ӧ���ﵽƽ��ʱ�������������Ϊԭ����1.25 ����ƽ��ʱˮ������ת����Ϊ25%����������в��� a mol ̿��ˮ������ת���ʽ����䣨���������С���������䡱�����ٲ��� a mol ˮ���� ��H218O��������������C16O��C18O �����ʵ���֮��Ϊ1��a��
��3����֪��C ��s��+$\frac{1}{2}$O2��g���TCO ��g������H=-110.5kJ•mo1-1
CO��g��+$\frac{1}{2}$O2��g���TCO2 ��g������H=-283.0kJ•mo1-1
H2 ��g��+$\frac{1}{2}$O2 ��g���TH2O ��g������H=-241.8kJ•mo1-1
��ô����2.4g ̿��ȫת��Ϊˮú����Ȼ����ȼ�գ��������̡�H=-78.7kJ•mo1-1��
C ��s��+H2O��g��?CO ��g��+H2 ��g������H=+131.3kJ•mol-1
��1��ij�¶��£��ĸ������о�������������Ӧ����������̿�������������ʵ����ʵ���Ũ�ȼ����淴Ӧ���ʹ�ϵ���±���ʾ������д������Ӧ�Ŀո�
| ������� | c��H2O��/mol•L-1 | c��CO��/mol•L-1 | c��H2��/mol•L-1 | V����V���Ƚ� |
| �� | 0.06 | 0.60 | 0.10 | V��=V�� |
| �� | 0.06 | 0.50 | 0.40 | �� |
| �� | 0.12 | 0.40 | 0.80 | V����V�� |
| �� | 0.12 | 0.30 | �� | V��=V�� |
��3����֪��C ��s��+$\frac{1}{2}$O2��g���TCO ��g������H=-110.5kJ•mo1-1
CO��g��+$\frac{1}{2}$O2��g���TCO2 ��g������H=-283.0kJ•mo1-1
H2 ��g��+$\frac{1}{2}$O2 ��g���TH2O ��g������H=-241.8kJ•mo1-1
��ô����2.4g ̿��ȫת��Ϊˮú����Ȼ����ȼ�գ��������̡�H=-78.7kJ•mo1-1��
7�����������У�������ǣ�������
| A�� | ������ˮ��ʹ��ɫʯ����Һ�ȱ�����ɫ | |
| B�� | ʵ������ȡ����ʱ�����ñ���ʯ��ˮ�����ն�������� | |
| C�� | Ư����Ư��ʱ���������ᣬ����Ư����ʹȼ�ϵ��л�ɫ����ɫ | |
| D�� | ��Ԫ����ɫ��Ӧ�IJ����ǣ�����˿����ϡ������ϴ�Ӻ���������ɫ��Ȼ�����ò�˿պȡ�����Ȼ��أ�����ú���ƵĻ����Ͻ������գ�����ɫ�ܲ������й۲� |
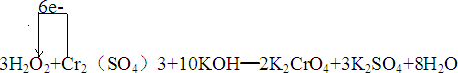 ��
�� 