题目内容
9.已知NaHSO3溶液显酸性,溶液中存在以下平衡:HSO3-+H2O?H2SO3+OH- ①
HSO3-?H++SO32- ②
向0.1mol•L-1的NaHSO3溶液中分别加入少量氢氧化钠固体,则$\frac{c(S{O}_{3}^{2-})}{c(HS{O}_{3}^{-})}$增大(填“增大”、“减小”或“不变”下同).$\frac{c(N{a}^{+})}{c(S{{O}_{3}}^{2-})}$增大.
分析 加入氢氧化钠,消耗溶液中的氢离子,促进电离平衡右移,抑制水解平衡,据此分析.
解答 解:加入氢氧化钠,消耗溶液中的氢离子,促进电离平衡右移,则c(SO32-)增大,所以$\frac{c(S{O}_{3}^{2-})}{c(HS{O}_{3}^{-})}$的值增大,加NaOH,溶液中钠离子浓度增大,由于钠离子浓度增大的程度大于c(SO32-)增大程度,所以溶液中 $\frac{c(N{a}^{+})}{c(S{{O}_{3}}^{2-})}$ 的值增大;
故答案为:增大;增大.
点评 本题考查电解质溶液,涉及弱电解质的电离和盐类的水解,注意把握影响弱电解质电离平衡的因素和影响盐的水解平衡的因素,题目难度不大,侧重于考查学生的分析能力.

练习册系列答案
相关题目
19.2010年10月16日,一场大雾袭击了京珠高速,导致京珠高速东西湖段接连发生数十起连环车祸.其中雾属于下列分散系中的( )
| A. | 溶液 | B. | 悬浊液 | C. | 乳浊液 | D. | 胶体 |
4.有a%、b%的氨水溶液和硫酸溶液,按下图所示混合,得到甲、乙、丙、丁四种溶液:四种溶液的密度由大到小的顺序为( )

| A. | 甲、乙、丙、丁 | B. | 丙、丁、乙、甲 | C. | 丙、丁、甲、乙 | D. | 丁、丙、乙、甲 |
4. 氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②,有关物质产率与温度的关系如图
氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②,有关物质产率与温度的关系如图
4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-905kJ?mol-1 ①
4NH3(g)+3O2(g)?2N2(g)+6H2O(g)△H=-1268kJ?mol-1 ②
下列说法中正确的是( )
 氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②,有关物质产率与温度的关系如图
氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②,有关物质产率与温度的关系如图4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-905kJ?mol-1 ①
4NH3(g)+3O2(g)?2N2(g)+6H2O(g)△H=-1268kJ?mol-1 ②
下列说法中正确的是( )
| A. | 在400℃时,反应①未达平衡,反应②达到平衡 | |
| B. | 800℃后再升高温度,反应①的平衡逆向移动;反应②的平衡正向移动 | |
| C. | 加压可提高NH3生成NO的转化率 | |
| D. | N2氧化为NO的热化学方程式为:N2(g)+O2(g)?2NO(g)△H=-181.5 kJ•mol-1 |
11.下列说法正确的是( )
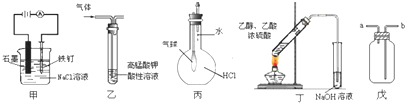
①装置甲可以防止铁钉生锈
②装置乙可除去乙烯中混有的乙炔
③装置丙可以验证HCl在水中的溶解性
④装置丁可用于实验室制取乙酸乙酯
⑤装置戊可用于收集H2、CO2、HCl、NO2等气体.

①装置甲可以防止铁钉生锈
②装置乙可除去乙烯中混有的乙炔
③装置丙可以验证HCl在水中的溶解性
④装置丁可用于实验室制取乙酸乙酯
⑤装置戊可用于收集H2、CO2、HCl、NO2等气体.
| A. | ①⑤ | B. | ②③ | C. | ③⑤ | D. | ④⑤ |
9.清晨松林中的空气格外清新,是因为有极少量的氧气变成了臭氧,反应的化学方程式为:3O2=2O3.太阳初升时,我们还会看到林中有光亮“通路”,下列有关说法正确的是( )
| A. | 上述反应为化合反应 | |
| B. | “通路”是胶体对光产生的丁达尔现象 | |
| C. | 上述反应为氧化还原反应 | |
| D. | 产生的臭氧有毒,会严重影响人体健康 |

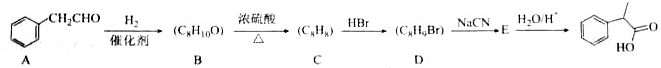
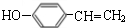 .
.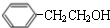 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$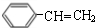 +H2O;C→D的反应类型为加成反应
+H2O;C→D的反应类型为加成反应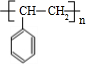 .
. 某位同学在查阅资料时发现含氮化合物有以下性质:
某位同学在查阅资料时发现含氮化合物有以下性质: