题目内容
11.下列离子方程式中书写正确的是( )| A. | FeCl2溶液中通入Cl2:Fe2++Cl2→Fe3++2Cl- | |
| B. | H2S通入CuSO4溶液中:Cu2++S2-→CuS↓ | |
| C. | FeS固体放人稀盐酸溶液中:FeS+2H+→Fe2++H2S↑ | |
| D. | AlCl3溶液中加入过量氨水:Al3++4OH-→AlO2-+2H2O |
分析 A.离子方程式两边总电荷不相等,违反了电荷守恒;
B.硫化氢为气体,离子方程式中不能拆开;
C.硫化亚铁与稀盐酸反应生成氯化亚铁和氯化氢;
D.氨水为弱碱,一水合氨不能拆开.
解答 解:A.FeCl2溶液中通入Cl2,反应生成氯化铁,正确的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,故A错误;
B.H2S通入CuSO4溶液中,反应生成硫化铜沉淀和硫酸,正确的离子方程式为:Cu2++H2S=CuS↓+2H+,故B错误;
C.FeS固体放人稀盐酸溶液中,反应生成氯化亚铁和硫化氢,反应的离子方程式为:FeS+2H+=Fe2++H2S↑,故C正确;
D.AlCl3溶液中加入过量氨水,反应生成氢氧化铝沉淀和氯化铵,正确的离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故D错误;
故选C.
点评 本题考查了离子方程式的判断,题目难度不大,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)等.

练习册系列答案
相关题目
12.Q、W、X、Y、Z是原子序数依次增大的短周期元素,Q和Y均满足主族序数与周期序数相等,Q与X、W与Z同主族,Q和W能形成原子个数之比为1:1和2:1的常见化合物.下列说法正确的是( )
| A. | 原子半径:Z>Y>X>W>Q | |
| B. | Q、X形成的化合物的电子式为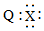 | |
| C. | 最简单氢化物的稳定性:Z>W | |
| D. | 工业上常用电解的方法制备X、Y的单质 |
2.下列化合物不能由单质之间直接化合得到的是( )
| A. | FeS | B. | SO3 | C. | FeCl3 | D. | NH3 |
19.下列除杂方案中,括号内为除去杂质所需的药品,其中正确的是( )
| A. | NaOH溶液中混有Ba(OH)2(CuSO4) | B. | Cu(NO3)2溶液中混有AgNO3(铜粉) | ||
| C. | CO2中混有CO(炽热的炭) | D. | CO2中混有HCl气体(NaOH溶液) |
16.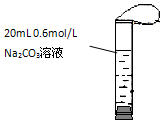 如图,将2mL浓度为6mol/L的盐酸用注射器通过橡皮塞慢慢注入,玻璃管中出现小气泡,气泡在溶液中逐渐上升的过程中消失.对该反应过程的推断不合理的是:( )
如图,将2mL浓度为6mol/L的盐酸用注射器通过橡皮塞慢慢注入,玻璃管中出现小气泡,气泡在溶液中逐渐上升的过程中消失.对该反应过程的推断不合理的是:( )
 如图,将2mL浓度为6mol/L的盐酸用注射器通过橡皮塞慢慢注入,玻璃管中出现小气泡,气泡在溶液中逐渐上升的过程中消失.对该反应过程的推断不合理的是:( )
如图,将2mL浓度为6mol/L的盐酸用注射器通过橡皮塞慢慢注入,玻璃管中出现小气泡,气泡在溶液中逐渐上升的过程中消失.对该反应过程的推断不合理的是:( )| A. | 有反应CO32-+2H+→CO2↑+H2O | |
| B. | 有反应CO32-+H+→HCO3-发生 | |
| C. | 有反应CO32-+CO2+H2O→2HCO3-发生 | |
| D. | 加快盐酸注入速度不会改变反应现象 |
3.最近医学界发现一种14C的羧酸衍生物在特定的条件下可通过断裂DNA杀死细胞,从而抑 制艾滋病,则下列关于14C的叙述正确的是( )
| A. | 其原子核内有8个中子 | B. | 是C60的同素异形体 | ||
| C. | 是14N的同素异形体 | D. | 与C60互为同位素 |
20.以下电离方程式错误的是( )
| A. | MgCl2═Mg2++2Cl- | B. | Fe2(SO4)3═2Fe3++3SO42- | ||
| C. | NaHCO3═Na++H++CO32- | D. | KHSO4═K++H++SO42- |