题目内容
2.下列化合物不能由单质之间直接化合得到的是( )| A. | FeS | B. | SO3 | C. | FeCl3 | D. | NH3 |
分析 A.硫氧化性较弱,与铁反应生成亚铁盐;
B.硫和氧气反应生成二氧化硫;
C.氯气具有强氧化性;
D.氮气和氢气在催化作用下反应生成氨气.
解答 解:A.硫氧化性较弱,与铁反应生成FeS,故A不选;
B.硫和氧气反应生成二氧化硫,二氧化硫和氧气在催化作用下生成三氧化硫,故B选;
C.氯气具有强氧化性,可与铁反应生成FeCl3,故C不选;
D.氮气和氢气在催化作用下反应生成氨气,故D不选.
故选B.
点评 本题考查物质的性质及应用,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,注意氧化还原反应的应用,题目难度不大.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
3.下列说法正确的是( )
| A. | 玻璃容器可长期盛放各种酸 | |
| B. | 不能用浸泡过高锰酸钾溶液的硅藻土保鲜水果 | |
| C. | 食品保鲜膜、塑料水杯等生活用品的主要成分是聚氯乙烯 | |
| D. | 轮船水线以下的船壳上装有锌块能减缓船壳的腐蚀 |
4.下列离子方程式书写正确的是( )
| A. | 硫酸铜溶液吸收H2S:Cu2++S2-═CuS↓ | |
| B. | 磁性氧化铁溶于氢碘酸:Fe3O4+8H+═Fe2++2Fe3++4H2O | |
| C. | 向饱和碳酸钠溶液中通入足量CO2:CO32-+CO2+H2O═2HCO3- | |
| D. | 向KAl(SO4)2溶液中加入过量的Ba(OH)2溶液:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O |
10.化学与生产、生活密切相关,下列事实的解释正确的是 ( )
| 选项 | 事实 | 解释 |
| A | 酸雨的pH<5.6 | CO2溶解在雨水中 |
| B | 稻草、甘蔗渣可用来造纸 | 稻草、甘蔗渣富含纤维素 |
| C | 化石燃料燃烧时采取固硫措施 | 提高化石燃料的利用率 |
| D | 将水中的铁闸门连接电源的负极而防腐 | 利用牺牲阳极的阴极保护法 |
| A. | A | B. | B | C. | C | D. | D |
17.某校化学课题组探究以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3•6H2O)的工艺,他们设计的流程如图所示,在“焙烧“过程中铁元素转 为 Fe3O4.下列推断正确的是( )
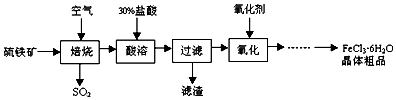

| A. | “焙烧”反应中,氧化产物是SO2,还原产物是Fe3O4 | |
| B. | “酸溶”时的酸可以用稀硫酸代替 | |
| C. | “过滤“后的滤液中Fe3+和Fe2+的浓度比为2:1 | |
| D. | “氧化”时的氧化剂只能选取Cl2 |
7.下列有关Cl、N、S等非金属元素化合物的说法正确的是( )
| A. | 漂白粉是纯净物,其成分就是次氯酸钙 | |
| B. | 实验室可用浓硫酸干燥氨气 | |
| C. | 实验室可用NaOH溶液处理SO2和HCl废气 | |
| D. | 浓盐酸、浓硫酸、浓硝酸都有强氧化性,能氧化金属铜 |
14.下列物质类型中,前者包括后者的是( )
| A. | 溶液、分散系 | B. | 氧化物、化合物 | C. | 溶液、胶体 | D. | 化合物、电解质 |
11.下列离子方程式中书写正确的是( )
| A. | FeCl2溶液中通入Cl2:Fe2++Cl2→Fe3++2Cl- | |
| B. | H2S通入CuSO4溶液中:Cu2++S2-→CuS↓ | |
| C. | FeS固体放人稀盐酸溶液中:FeS+2H+→Fe2++H2S↑ | |
| D. | AlCl3溶液中加入过量氨水:Al3++4OH-→AlO2-+2H2O |
12.下列实验方法或者结论不正确的是( )
| A. | 甲同学准确称取5.0gNaCl配制一定物质的量浓度的溶液时,乙同学发现NaCl固体与砝码放反了,但乙同学认为这个错误操作对实验结果没有影响 | |
| B. | 做酯化反应反应混合液的配制应先加乙醇,再加浓硫酸,冷却后最后加入乙酸 | |
| C. | 洗涤沉淀的方法是直接向过滤器中加入适量蒸馏水,然后让水自然流下 | |
| D. | 要检验滴有稀硫酸的蔗糖溶液是否水解,可加入银氨溶液,再水浴加热 |