题目内容
铜钱在历史上曾经是一种广泛流通的货币.试从物理性质和化学性质的角度分析为什么铜常用于制造货币.(铜的熔点是1183.4℃,铁的熔点是1534.8℃.)
考点:铜金属及其重要化合物的主要性质
专题:金属概论与碱元素
分析:结合题目中所给出的信息,根据铜与铁相比具有的优点解答.
解答:
解:铜的熔点是1183.4℃、铁的熔点是1534.8℃,说明铜的熔点比铁的熔点低,便于铸造;货币流通的次数比较多,所以要防止生锈,铁比铜易锈蚀,
答:因为铜的熔点比铁的低易于铸造,铁比铜易锈蚀.
答:因为铜的熔点比铁的低易于铸造,铁比铜易锈蚀.
点评:本题考查金属铁、铜的性质,掌握铁腐蚀的原理为解答的关键,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
标准状体下,用质量相同的4种气体吹气球,那种气体吹起的气球体积最大( )
| A、O2 |
| B、H2 |
| C、CH4 |
| D、CO2 |
在密闭容器中,将1.0mol CO与1.0mol H2O混合加热到800℃,发生下列反应:CO(g)+H2O(g)?CO2(g)+H2(g).一段时间后该反应达到平衡,测得CO的物质的量为0.5mol.则下列说法正确的是( )
| A、800℃下,该反应的化学平衡常数为0.25 |
| B、427℃时该反应的平衡常数为9.4,则该反应的△H<0 |
| C、800℃下,若继续向该平衡体系中通入1.0mol的CO(g),则平衡时CO物质的量分数为33.3% |
| D、800℃下,若继续向该平衡体系中通入1.0mol的H2O(g),则平衡时CO转化率为33.3% |
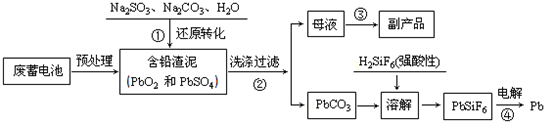
铜有两种常见的氧化物CuO和Cu2O.某学习小组取0.98g(用精密天平测量)Cu(OH)2固体加热,有铜的氧化物生成,其质量随温度变化如图1所示:另外,某同学绘制了三条表示金属氧化物与其所含金属元素的质量的关系曲线,如图2所示.则下列分析正确的是( )

| A、图1中,A到B的过程中有0.01 mol电子发生了转移 |
| B、图1整个过程中共生成0.26 g水 |
| C、图2三条曲线中,表示CuO和其中所含Cu元素质量关系的曲线是A |
| D、图1中A和B化学式分别为Cu2O和CuO |
 请用如图的装置设计一个实验,以测定SO2转化为SO3的转化率.
请用如图的装置设计一个实验,以测定SO2转化为SO3的转化率.