题目内容
20.反应A+B→C(△H<0)分两步进行:①A+B→X(△H>0),②X→C(△H<0).下列示意图中,能正确表示总反应过程中能量变化的是( )| A. | 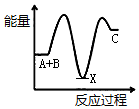 | B. | 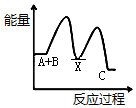 | C. | 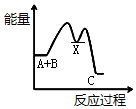 | D. | 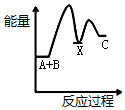 |
分析 反应物总能量大于生成物总能量时为放热反应,反之为吸收反应,结合总反应、分步反应中能量变化及图象判断,以此来解答.
解答 解:A+B→C为放热反应,则A+B的总能量大于生成C的总能量,排除选项A、D,A+B→X(吸热),则X的能量大于A+B的总能量,X→C(放热),则X的能量大于C的总能量,排除选项B,
故选C.
点评 本题考查反应热与焓变,为高频考点,把握反应中能量变化、吸热与放热反应的判断为解答的关键,侧重分析与应用能力的考查,注意排除法应用,题目难度不大.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案
相关题目
11.下列化合物中,既存在离子键又存在共价键的是( )
| A. | 硫酸钠 | B. | 乙酸 | C. | 氯化镁 | D. | 二氧化碳 |
8.西瓜膨大剂别名氯吡苯脲,是经过国家批准的植物生长调节剂,实践证明长期使用对人体无害.已知其相关性质如表所示:
(1)氯元素基态原子核外电子的成对电子数为16,氯吡苯脲中所含元素能形成10电子分子,且分子之间能形成氢键的有NH3、H2O.(填二种,填化学式)
(2)氯吡苯脲的晶体类型为分子晶体.该分子是由极性、非极性键形成的极性分子(填“极性”或“非极性”)
| 分子式 | 结构简式 | 外观 | 熔点 | 溶解性 |
| C12H10ClN3O | 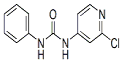 | 白色结晶粉末 | 170~172°C | 易溶于水 |
(2)氯吡苯脲的晶体类型为分子晶体.该分子是由极性、非极性键形成的极性分子(填“极性”或“非极性”)
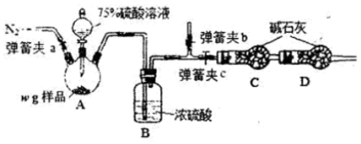
5.用下列装置完成相关实验,合理的是( )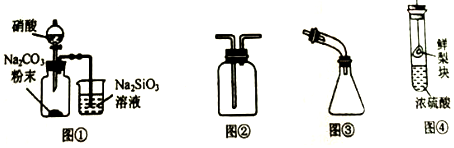

| A. | 图①:证明非金属性由强到弱的顺序是N>C>Si | |
| B. | 图②:收集NO2或NH3 | |
| C. | 图③:海水蒸馏时接收蒸馏水 | |
| D. | 图④:探究浓硫酸的脱水性 |
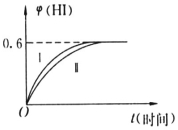 将1molI2(g)和2molH2(g)置于某2L密闭容器中,在一定温度下发生反应:I2(g)+H2(g)?2HI(g)△H<0,并在10min时达到平衡.HI的体积分数φ(HI)随时间变化如图所示曲线(Ⅱ).
将1molI2(g)和2molH2(g)置于某2L密闭容器中,在一定温度下发生反应:I2(g)+H2(g)?2HI(g)△H<0,并在10min时达到平衡.HI的体积分数φ(HI)随时间变化如图所示曲线(Ⅱ).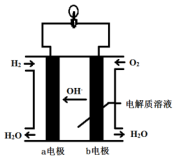 英国一家公司正在研发全球首款“充一次电,用七天”的碱性氢氧燃料手机电池.如图为碱性氢氧燃料电池结构示意图.
英国一家公司正在研发全球首款“充一次电,用七天”的碱性氢氧燃料手机电池.如图为碱性氢氧燃料电池结构示意图.