题目内容
NA为阿伏加德罗常数,下列叙述中正确的是( )
①106gNaCO3晶体中的离子总数大于3NA
②标准状况下,16gO3和O2混合气体中含有的氧原子数为为NA
③将0.1molNaCl全部溶于乙醇中制成胶体,其中含有的胶体粒子数目为0.1NA
④1molCl2与足量水反应后生成的HClO分子数小于1NA.
①106gNaCO3晶体中的离子总数大于3NA
②标准状况下,16gO3和O2混合气体中含有的氧原子数为为NA
③将0.1molNaCl全部溶于乙醇中制成胶体,其中含有的胶体粒子数目为0.1NA
④1molCl2与足量水反应后生成的HClO分子数小于1NA.
| A、①② | B、②④ | C、①③ | D、③④ |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:①根据微粒数N=nNA=
×NA来计算;
②O3和O2都是由氧原子构成,故氧原子的质量为16g,根据n=
计算氧原子的物质的量,再根据N=nNA计算氧原子数目;
③胶体粒子是多个微粒的集合体;
④次氯酸为弱电解质,部分电离.
| m |
| M |
②O3和O2都是由氧原子构成,故氧原子的质量为16g,根据n=
| m |
| M |
③胶体粒子是多个微粒的集合体;
④次氯酸为弱电解质,部分电离.
解答:
解:①1mol碳酸钠晶体中含有2mol钠离子和1mol碳酸根离子,根据微粒数N=nNA=
×3NA=3NA,故①错误;
②16gO3和O2混合气体中氧原子的质量为16g,故n(O)=
=1mol,含有的氧原子数为1mol×NAmol-1=NA,故②正确;
③由于胶体粒子是多个微粒的集合体,所含的胶体粒子数目小于0.1 NA,故③错误;
④1molCl2与足量水反应后生成的HClO分子的物质的量为1mol,但是次氯酸为弱电解质,部分电离,所以生成的次氯酸分子数小于1NA,故④正确;
故选:B.
| 106g |
| 106g/mol |
②16gO3和O2混合气体中氧原子的质量为16g,故n(O)=
| 16g |
| 16g/mol |
③由于胶体粒子是多个微粒的集合体,所含的胶体粒子数目小于0.1 NA,故③错误;
④1molCl2与足量水反应后生成的HClO分子的物质的量为1mol,但是次氯酸为弱电解质,部分电离,所以生成的次氯酸分子数小于1NA,故④正确;
故选:B.
点评:本题考查了阿伏伽德罗常数的应用,主要考查质量换算物质的量计算微粒数,胶体粒子的实质,可逆反应的判断应用.

练习册系列答案
 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案
相关题目
下列反应不属于取代反应的是( )
| A、CHCl3+HF→CHFCl2+HCl | |||
B、2CH3CH2OH
| |||
| C、H2C=CH2+Br2→CH2Br-CH2Br | |||
D、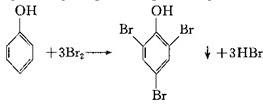 |
对于锌-铜-稀H2SO4组成的原电池装置中,当导线中有1mol电子通过时,理论上的电极变化是( )
①锌片溶解了32.5g②锌片增重32.5g③铜片上析出了1gH2④铜片上析出1mol H2⑤溶液中的SO42-移向锌极⑥溶液中SO42-移向铜极.
①锌片溶解了32.5g②锌片增重32.5g③铜片上析出了1gH2④铜片上析出1mol H2⑤溶液中的SO42-移向锌极⑥溶液中SO42-移向铜极.
| A、①③⑤ | B、①④⑥ |
| C、②③⑤ | D、②④⑥ |
下列化学用语表述正确的是( )
A、“84消毒液”中有效成分NaCIO的电子式:Na+[
| ||||||||||||||
B、食盐中阴离子的核外电子排布式: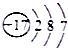 | ||||||||||||||
C、聚丙烯的结构简式: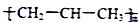 | ||||||||||||||
| D、乙烯的结构简式:CH2CH2 |
设NA表示阿伏加德罗常数的值.下列有关说法正确的是( )
| A、在标准状况下,2.24L氦气含有共用电子对数的0.5NA |
| B、22.4g铁粉完全溶于一定浓度的硝酸中,转移的电子数可能为0.6NA |
| C、4.6g甲醇和二甲醚(CH3-O-CH3)的混合物中所含分子数等于0.1NA |
| D、含Al3+数目为0.1NA的硝酸铝溶液中,NO3-个数大于NA |
下列离子方程式的书写正确的是( )
| A、铁和稀盐酸反应:2Fe+6H+═2Fe3++3H2↑ |
| B、用小苏打治疗胃酸过多反应:CO32-+2H+═CO2↑+H2O |
| C、实验室用大理石跟盐酸反应:CO32-+2H+═CO2↑+H2O |
| D、向Ba(OH)2溶液中滴加H2SO4溶液反应:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O |
 如图所示将2mol SO2和1mol O2混合置于体积可变的等压容器中,在一定温度下发生如下反应:2SO2(g)+O2(g)?2SO3(g);△H<0.该反应达到平衡状态A时,测得气体总物质的量为2.4mol.若SO2、O2、SO3的起始物质的量分别用a、b、c 表示,回答下列问题:
如图所示将2mol SO2和1mol O2混合置于体积可变的等压容器中,在一定温度下发生如下反应:2SO2(g)+O2(g)?2SO3(g);△H<0.该反应达到平衡状态A时,测得气体总物质的量为2.4mol.若SO2、O2、SO3的起始物质的量分别用a、b、c 表示,回答下列问题: