题目内容
1.元素的原子结构决定其性质和在周期表中的位置.下列说法正确的是( )| A. | 所有元素原子的最外层电子数都等于元素的最高化合价 | |
| B. | P、S、Cl得电子能力和最高价氧化物对应的水化物的酸性均依次减弱 | |
| C. | 多电子原子中,在离核较近的区域内运动的电子能量较高 | |
| D. | 熔融状态能导电的化合物一定含有离子键 |
分析 A.主族元素原子的最外层电子数等于元素的最高化合价数,但O、F元素除外;
B.原子核外最外层电子数越多,该原子得电子能力越强,其最高价氧化物的水化物酸性越强;
C.多电子原子中,在离核越近的区域内运动的电子能量越低;
D.含有离子键的化合物是离子化合物,熔融状态下含有自由移动离子的化合物能导电.
解答 解:A.主族元素原子的最外层电子数等于元素的最高化合价数,但O、F元素除外,O、F元素没有正化合价,故A错误;
B.原子核外最外层电子数越多,该原子得电子能力越强,其最高价氧化物的水化物酸性越强,P、S、Cl原子最外层电子数依次增多,所以其得电子能力和最高价氧化物对应的水化物的酸性均依次增强,故B错误;
C.多电子原子中,在离核越近的区域内运动的电子能量越低,离核越远的电子能量越高,故C错误;
D.含有离子键的化合物是离子化合物,熔融状态下含有自由移动离子的化合物能导电,所以熔融状态能导电的化合物一定是离子化合物,故D正确;
故选D.
点评 本题考查元素周期表结构和性质、元素周期律、元素周期表的应用等知识点,明确元素周期律内涵、元素性质、原子结构及元素周期表结构特点即可解答,注意规律中的异常现象,异常现象是A.

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
11.用已知浓度的酸滴定未知浓度的碱时,用甲基橙作指示剂,会导致待测碱液的浓度偏低的操作是( )
①酸式滴定管用蒸馏水洗后,未用标准液润洗
②碱式滴定管用蒸馏水洗后,未用待测液润洗
③锥形瓶用蒸馏水洗后,用待测夜润洗
④滴定前酸式滴定管尖嘴部分有气泡,滴定完成后气泡消失
⑤滴定中不慎将锥形瓶内液体摇出少量于瓶外.
①酸式滴定管用蒸馏水洗后,未用标准液润洗
②碱式滴定管用蒸馏水洗后,未用待测液润洗
③锥形瓶用蒸馏水洗后,用待测夜润洗
④滴定前酸式滴定管尖嘴部分有气泡,滴定完成后气泡消失
⑤滴定中不慎将锥形瓶内液体摇出少量于瓶外.
| A. | ①③④ | B. | ②⑤ | C. | ②③⑤ | D. | ②④ |
9.用系统命名法给下列有机物命名,其中正确的是( )
| A. | 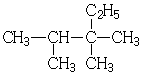 2,3-二甲基-3-乙基丁烷 | B. | 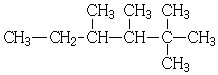 2,2,3,4-四甲基己烷 | ||
| C. |  对二甲苯 | D. |  2,4,4-三甲基戊烯 |
16.某同学设计下列方法对A盐的水溶液进行鉴定:
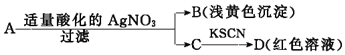
由此得出的结论中,不正确的是( )

由此得出的结论中,不正确的是( )
| A. | D溶液中存在Fe(SCN)3 | B. | 滤液C中有Fe3+ | ||
| C. | B为AgBr | D. | A一定是FeBr2 |
6.已知氯气、溴蒸气分别跟氢气反应的热化学方程式如下(Q1、Q2均为正值):H2(g)+Cl2(g)-→2HCl(g)+Q1H2(g)+Br2(g)-→2HBr(g)+Q2有关上述反应的叙述正确的是( )
| A. | Q1>Q2 | |
| B. | 生成物总能量均高于反应物总能量 | |
| C. | 生成1 mol HCl气体时放出Q1 kJ热量 | |
| D. | 1 mol HBr(g)具有的能量小于1 mol HBr(l)具有的能量 |
13.钫(Fr)元素在周期表中位于第七周期,第IA族,根据钫在周期表中的位置推测其性质,其中错误的是
( )
( )
| A. | 其单质的熔点比钠的熔点低 | B. | 在空气中燃烧只能生成Fr2O | ||
| C. | 其原子半径在同一主族中是最大的 | D. | 氧化物对应的水化物的碱性很强 |
10.我国科学家研发出一种新型的锂离子电池,放电时有关离子转化关系如图所示,下列说法正确的是( )
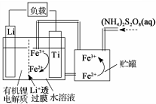

| A. | Li+透过膜除允许Li+通过外,还允许H2O分子通过 | |
| B. | 放电时,进入贮罐的液体发生:S2O82-+2Fe2+=2Fe3++2SO42- | |
| C. | 充电时,钛电极与外电源的负极相连 | |
| D. | 充电时,电池内部发生的总反应为Li++Fe3+=Li+Fe2+ |