题目内容
A、B、C、D四种元素核电荷数均小于18.B元素是地壳中含量最多的元素,A、C元素的原子最外层电子数相等,C、D元素原子电子层数相同.A原子最外层电子数等于电子层数,C原子最外层电子数是K层上电子数的一半.D元素原子有三个电子层,D-离子电子层结构与氩原子电子层结构相同.则四种元素的名称为:
(1)A B C D ;
(2)A原子、C+离子的结构示意图为 、 ;
(3)B原子、D-离子的电子式为 , ;
(4)A单质与B单质的化学方程式为 .
(1)A
(2)A原子、C+离子的结构示意图为
(3)B原子、D-离子的电子式为
(4)A单质与B单质的化学方程式为
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:B元素是地壳中含量最多的元素,所以B是氧元素,C原子最外层电子数是K层上电子数的一半,即最外层电子数是1,是第ⅠA族元素,A、C元素的原子最外层电子数相等,A原子最外层电子数等于电子层数,所以A是氢元素,C、D元素原子电子层数相同,D元素原子有三个电子层,所以C是钠元素.D-离子电子层结构与氩原子电子层结构相同,则D是氯元素.在确定了元素种类之后可作解答.
解答:
解:B元素是地壳中含量最多的元素,所以B是氧元素,C原子最外层电子数是K层上电子数的一半,即最外层电子数是1,是第ⅠA族元素,A、C元素的原子最外层电子数相等,A原子最外层电子数等于电子层数,所以A是氢元素,C、D元素原子电子层数相同,D元素原子有三个电子层,所以C是钠元素.D-离子电子层结构与氩原子电子层结构相同,则D是氯元素.
(1)由上面的分析可知A是氢元素,B是氧元素,C是钠元素,D是氯元素,故答案为:氢,氧,钠,氯;
(2)A原子为氢原子,它的原子结构示意图为: ,D-为氯离子,它的结构示意图为:
,D-为氯离子,它的结构示意图为: ,故答案为:
,故答案为: ,
, (3)B原子是氧原子,它电子式为:
(3)B原子是氧原子,它电子式为: ,D-离子是氯离子,它的电子式为
,D-离子是氯离子,它的电子式为 ,故答案为:
,故答案为: ,
, ;
;
(4)A元素是氢元素,它的单质是氢气,B元素是氧元素,它的单质是氧气,H2、O2反应的化学方程式为2H2+O2
2H2O,故答案为:2H2+O2
2H2O.
(1)由上面的分析可知A是氢元素,B是氧元素,C是钠元素,D是氯元素,故答案为:氢,氧,钠,氯;
(2)A原子为氢原子,它的原子结构示意图为:
 ,D-为氯离子,它的结构示意图为:
,D-为氯离子,它的结构示意图为: ,故答案为:
,故答案为: ,
, (3)B原子是氧原子,它电子式为:
(3)B原子是氧原子,它电子式为: ,D-离子是氯离子,它的电子式为
,D-离子是氯离子,它的电子式为 ,故答案为:
,故答案为: ,
, ;
;(4)A元素是氢元素,它的单质是氢气,B元素是氧元素,它的单质是氧气,H2、O2反应的化学方程式为2H2+O2
| ||
| ||
点评:本题考查了学生根据元素原子结构推导元素种类的能力,并根据推出的元素回答相关问题,本题推导元素有一定的难度,问的问题则较简单.总体难度中等.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
具有下列电子排布式的原子中,原子半径最大的是( )
| A、1s22s22p63s23p2 |
| B、1s22s22p63s2 |
| C、1s22s22p2 |
| D、1s22s22p63s23p4 |
下列说法正确的是( )
| A、H2O和H2O2中的化学键类型完全相同 |
| B、N2的结构式为N-N |
| C、一个H2O分子所含的中子数为8(质量数:H-1,O-16) |
D、NaCl的电子式为 |
下列说法中正确的是( )
| A、醇在Cu或Ag的催化作用下都可以氧化成醛 |
B、有机物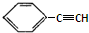 的所有原子一定处于同一平面上 的所有原子一定处于同一平面上 |
| C、醇都可以在浓H2SO4作用下以及170℃时发生消去反应 |
| D、分子组成相差一个或几个CH2原子团的化合物必定互为同系物 |