题目内容
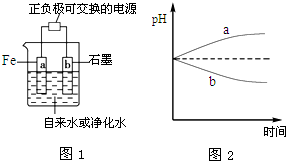 推销净水器的商人用自来水做电解实验,一段时间后两极间产生灰绿色沉淀,并很快变成红褐色,然后用净水器净化后的水做电解实验,两极上只有气体产生,水中并无沉淀,用以证明自来水很“脏”.人们将自来水送检,却是合格的,下列有关说法,合理的是( )
推销净水器的商人用自来水做电解实验,一段时间后两极间产生灰绿色沉淀,并很快变成红褐色,然后用净水器净化后的水做电解实验,两极上只有气体产生,水中并无沉淀,用以证明自来水很“脏”.人们将自来水送检,却是合格的,下列有关说法,合理的是( )| A、商人电解自来水时,用石墨做阳极;电解净化水时,用铁做阳极 |
| B、电解自来水时,阴极反应式:O2+2H2O+4e-═4OH- |
| C、电解净化水时,a、b两极的pH变化如图2所示 |
| D、电解自来水实验中,若阴极产生气体为3.36L(标况),则阳极质量减小5.6克 |
考点:电解原理
专题:
分析:A.电解自来水时生成或灰绿色的絮状物并很快变成红褐色,铁作阳极,石墨作阴极,电解净化水时,用石墨做阳极,用铁做阴极;
B.依据电解自来水时出现非常明显的灰绿色沉淀,说明电解过程中生成亚铁离子,铁做阳极失电子生成亚铁离子,石墨作阴极,氢离子得电子生成氢气;
C.电解净化水时用石墨做阳极,用铁做阴极,本质为电解水;
D.阴极生成为氢气,计算出氢气的物质的量,然后利用电子守恒计算出阳极减小的质量.
B.依据电解自来水时出现非常明显的灰绿色沉淀,说明电解过程中生成亚铁离子,铁做阳极失电子生成亚铁离子,石墨作阴极,氢离子得电子生成氢气;
C.电解净化水时用石墨做阳极,用铁做阴极,本质为电解水;
D.阴极生成为氢气,计算出氢气的物质的量,然后利用电子守恒计算出阳极减小的质量.
解答:
解:A.商人电解自来水时,用铁做阳极,阳极上铁失电子生成亚铁离子,亚铁离子和氢氧根离子反应生成白色沉淀氢氧化亚铁,氢氧化亚铁不稳定,易被氧化生成氢氧化铁,所以白色沉淀立即变为灰绿色,最终变为红褐色,电解净化水时,用石墨做阳极,本质为电解水,两极上只有气体产生,水中并无沉淀,故A错误;
B.电解自来水时,铁做阳极失电子生成亚铁离子,电极反应为;Fe-2e-=Fe2+,阴极电极反应为2H++2e-═H2↑,故B错误;
C.当电解器插入纯净水时,用石墨做阳极,用铁做阴极,b电极为阳极4OH--4e-=2H2O+O2↑,pH减小,a电极为阴极,2H++2e-═H2↑,pH增大,故C正确;
D.3.36L(标况)物质的量为n=
=0.15mol,电解自来水时,铁做阳极失电子生成亚铁离子,电极反应为;Fe-2e-=Fe2+,阴极电极反应为2H++2e-═H2↑,所以0.15mol为氢气,则溶解的铁为0.15mol,阳极减小的质量为0.15mol×56g/mol=8.4g,故D错误;
故选C.
B.电解自来水时,铁做阳极失电子生成亚铁离子,电极反应为;Fe-2e-=Fe2+,阴极电极反应为2H++2e-═H2↑,故B错误;
C.当电解器插入纯净水时,用石墨做阳极,用铁做阴极,b电极为阳极4OH--4e-=2H2O+O2↑,pH减小,a电极为阴极,2H++2e-═H2↑,pH增大,故C正确;
D.3.36L(标况)物质的量为n=
| 3.36L |
| 22.4L/mol |
故选C.
点评:本题以信息给予为载体考查了电解原理,根据实验现象知,电解自来水铁作阳极,石墨作阴极,电解净化水时,用石墨做阳极,用铁做阴极,理解过程和实质,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
下列溶液一定呈中性的是( )
A、c(OH-)=
| ||
| B、pH=7 的溶液 | ||
| C、c(H+)=10-14的溶液 | ||
| D、加甲基橙呈黄色的溶液 |
小华家中有如下生活用品:碘酒、食盐、食醋、84消毒液(内含NaClO),小华利用上述用品不能完成的任务是( )
| A、检验买来的奶粉中是否加有淀粉 |
| B、检验自来水中是否含有Cl- |
| C、除去保温瓶中的水垢 |
| D、洗去白色衣服上的番茄汁 |
下列图示所表示的实验设计正确的是( )
A、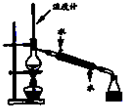 分离苯和甲苯 |
B、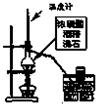 制备乙烯 |
C、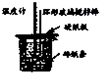 测定中和热 |
D、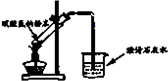 加入碳酸氢钠 |
人造象牙中,主要物质是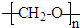 ,合成它的单体是( )
,合成它的单体是( )
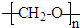 ,合成它的单体是( )
,合成它的单体是( )| A、CH3-O-CH3(甲醚) |
| B、HCHO(甲醛) |
| C、CH3CHO(乙醛) |
| D、HCOOH(甲酸) |
25℃时,1mol/L的NH4Cl、CH3COONH4、NH4HSO4、NH3?H2O四种溶液中,测得c(NH4+)分别为a、b、c、d(单位为mol/L),下列判断正确的是( )
| A、a=b=c=d |
| B、a>b>d>c |
| C、d>a>c>b |
| D、c>a>b>d |