题目内容
在三个密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)从小到大的是( )
| A、p (Ne)<p (H2)<p (O2) |
| B、p (O2)<p (Ne)<p (H2) |
| C、p (H2)<p (O2)<p (Ne) |
| D、p (H2)<p (Ne)<p (O2) |
考点:物质的量的相关计算
专题:计算题
分析:由PV=nRT=
RT,可得PM=ρRT,故在温度和密度都相同条件下,压强与摩尔质量呈反比.
| m |
| M |
解答:
解:由PV=nRT=
RT,可得PM=ρRT,故在温度和密度都相同条件下,压强与摩尔质量呈反比,
Ne的摩尔质量为20g/mol,H2的摩尔质量为2g/mol,O2的摩尔质量为32g/mol,
所以三种气体的压强(p)从大到小的顺序是p(O2)<p(Ne)<p(H2),
故选:B.
| m |
| M |
Ne的摩尔质量为20g/mol,H2的摩尔质量为2g/mol,O2的摩尔质量为32g/mol,
所以三种气体的压强(p)从大到小的顺序是p(O2)<p(Ne)<p(H2),
故选:B.
点评:考查阿伏伽德罗定律及推论,难度不大,可借助pV=nRT理解阿伏伽德罗定律及推论,注意稀有气体是单原子分子.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
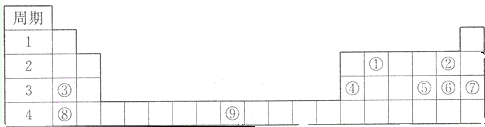
奥运五环代表着全世界五大洲的人民团结在一起.下列各项中的物质能满足如图中阴影部分关系的是( )


| A、①NaCl;②K2SO4;③KCl;④(NH4)2SO4; |
| B、①Na2SO4;②K2SO4;③KCl;④(NH4)2SO4; |
| C、①NaCl;②K2SO4;③KCl;④NH4Cl; |
| D、①Na2SO4;②K2SO4;③KCl;④NH4Cl. |
下列物质:①水泥 ②玻璃 ③陶瓷 ④水晶,其中属于硅酸盐工业产品的是( )
| A、只有①② | B、只有②④ |
| C、只有①②③ | D、全部 |
下列关于0.1mol/L硝酸钾溶液配制的说法中,错误的是( )
| A、0.05molKNO3溶于水配制成500mL水溶液 |
| B、0.01molKNO3溶于100mL水配制而成 |
| C、0.2mol/LKNO3溶液100mL稀释成200mL |
| D、0.1molKNO3溶于水配制成1L水溶液 |
以下实验操作正确的是( )
A、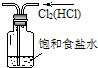 除去Cl2中的HCl气体 |
B、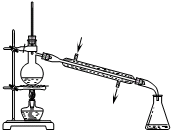 淡化海水 |
C、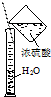 稀释浓硫酸 |
D、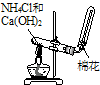 验室制取氨气 |