题目内容
下列关于0.1mol/L硝酸钾溶液配制的说法中,错误的是( )
| A、0.05molKNO3溶于水配制成500mL水溶液 |
| B、0.01molKNO3溶于100mL水配制而成 |
| C、0.2mol/LKNO3溶液100mL稀释成200mL |
| D、0.1molKNO3溶于水配制成1L水溶液 |
考点:溶液的配制
专题:化学实验基本操作
分析:0.1mol/L KNO3溶液的意义是:每1L溶液中含有KNO3的物质的量为0.1mol,注意1L是指溶液的体积,不是溶剂的体积.
解答:
解:A、溶液浓度c=
=
=0.1mol/L,故A正确;
B、0.01molKNO3溶于100mL水,是指的溶剂的体积为1L,而不是溶液的体积为1L,故B错误;
C、溶液浓度c=
=
=0.1mol/L,故C正确;
D、溶液浓度c=
=
=0.1mol/L,故D正确.
故选:B.
| n |
| V |
| 0.05mol |
| 0.5L |
B、0.01molKNO3溶于100mL水,是指的溶剂的体积为1L,而不是溶液的体积为1L,故B错误;
C、溶液浓度c=
| n |
| V |
| 0.2mol/L×0.1L |
| 0.2L |
D、溶液浓度c=
| n |
| V |
| 0.1mol |
| 1L |
故选:B.
点评:本题考查了一定物质的量浓度溶液的配制,难度不大,注意根据c=
理解溶液配制.
| n |
| V |

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案
相关题目
正确掌握好化学用语是学好化学的基础,下列有关表述正确物是( )
| A、乙烯的结构简式:CH2CH2 |
B、NH3的电子式: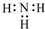 |
| C、NaHCO3水解的离子方程式:HCO3-+H2O?H3O++CO32- |
| D、亚硫酸氢根离子的电离方程式:HSO3-+H2O?H3O++SO32- |
20g某合金放入足量的稀盐酸中,产生标况下11.2L的氢气,则该合金可能是下列中的( )
| A、Al、Fe合金 |
| B、Mg、Ca合金 |
| C、Na、K合金 |
| D、Mg、Cu合金 |
下列变化属于吸热反应的是( )
| A、浓硫酸稀释 |
| B、液态水汽化 |
| C、生石灰跟水反应生成熟石灰 |
| D、将胆矾加热变为白色粉末 |
设NA代表阿伏加德罗常数,下列叙述正确的是( )
| A、标准状况下,11.2L的O2和NO的混合物含有的分子数约为0.5×6.02×1023 |
| B、1mol的羟基与1 mol的氢氧根离子所含电子数均为9 NA |
| C、常温常压下42g 乙烯和丁烯混合气体中,极性键数为6NA |
| D、6.4g SO2与足量氧气反应生成SO3,转移电子数为0.2NA |
在三个密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)从小到大的是( )
| A、p (Ne)<p (H2)<p (O2) |
| B、p (O2)<p (Ne)<p (H2) |
| C、p (H2)<p (O2)<p (Ne) |
| D、p (H2)<p (Ne)<p (O2) |
在同温同压下,下列各组热化学方程式中,△H2>△H1的是( )
| A、S(s)+O2(g)=SO2 (g);△H1 S(g)+O2(g)=SO2 (g);△H2 | ||||
| B、2H2(g)+O2 (g)=2H2O(g);△H1 2H2 (g)+O2 (g)=2H2O(l);△H2 | ||||
| C、CO(g)+1/2 O2(g)=CO2(g);△H1 2CO(g)+O2(g)=2CO2(g);△H2 | ||||
D、H2 (g)+Cl2(g)=2HCl(g);△H1
|
25℃时,下列溶液中水的电离程度最大的是( )
| A、0.01 mol/L盐酸 |
| B、0.01 mol/L Na2CO3溶液 |
| C、pH=4 的NaHSO3溶液 |
| D、pH=11氨水 |
绚丽的焰火将上海世博会开幕式推向了高潮.焰火与高中化学中“焰色反应”知识有关.下列有关“焰色反应”说法中正确的是( )
| A、焰色反应为化学变化 |
| B、所有金属及其化合物灼烧时火焰均有颜色 |
| C、NaCl与Na2CO3灼烧时火焰颜色相同 |
| D、焰色反应均应透过蓝色钴玻璃观察 |