题目内容
5.在标准状况下,在臭氧(O3)发生器中装入100mL O2,反应后的体积在标准状况下变为95mL,则在标准状况下,最终混合气体(只有臭氧和氧气)的密度是多少.分析 根据质量守恒定律可知,反应后混合气体的质量等于反应前氧气的质量,根据n=$\frac{V}{{V}_{m}}$计算反应前氧气的物质的量,在根据m=nM计算反应前氧气的质量,根据ρ=$\frac{m}{V}$计算混合气体的密度.
解答 解:反应前氧气的物质的量=$\frac{0.1L}{22.4L/mol}$=$\frac{1}{224}$mol,故反应前氧气的质量$\frac{1}{224}$mol×32g/mol=$\frac{1}{7}$g,根据质量守恒定律可知,反应后混合气体的质量等于反应前氧气的质量,故反应后混合气体的密度=$\frac{\frac{1}{7}g}{0.095L}$=1.5g/L,
答:标准状况下,最终混合气体的密度是1.5g/L.
点评 本题以密度计算为载体,考查化学方程式计算、物质的量的计算,关键是利用质量守恒定律计算混合气体质量,难度不大.

练习册系列答案
相关题目
16.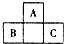 如图所示是元素周期表中短周期的一部分,已知B原子与C原子核外电子总数为A原子核外电子总数的4倍,则下列推断正确的是( )
如图所示是元素周期表中短周期的一部分,已知B原子与C原子核外电子总数为A原子核外电子总数的4倍,则下列推断正确的是( )
 如图所示是元素周期表中短周期的一部分,已知B原子与C原子核外电子总数为A原子核外电子总数的4倍,则下列推断正确的是( )
如图所示是元素周期表中短周期的一部分,已知B原子与C原子核外电子总数为A原子核外电子总数的4倍,则下列推断正确的是( )| A. | A、B、C三者均为非金属元素 | B. | B与C只能形成一种共价化合物 | ||
| C. | A与B、A与C均可形成离子化合物 | D. | A、B、C三者最外层电子数之和为40 |
13.下列与有机物的结构、性质有关的叙述正确的是( )
| A. | 分子式为C5H12O且可与金属钠反应放出氢气的有机物有4种 | |
| B. | 甲苯分子中所有原子可能共面 | |
| C. | 苯、乙醇、油脂均不能使酸性KMnO4溶液褪色 | |
| D. | C3H2Cl6有四种同分异构体 |
20.食品添加剂通常必须在一定范围内使用,否则会损害人体健康,滥用下列食品添加剂会导致癌症发生率增加的是( )
| A. | KIO3 | B. | 苯甲酸钠 | C. | 维生素E | D. | NaNO2 |
10.下列含有非极性键的共价化合物是( )
| A. | N2 | B. | Na2O2 | C. | N2H4 | D. | CH4 |
17.下列说法正确的是( )
| A. | NH4Cl固体为离子化合物 | |
| B. | CO2分子中含有离子健 | |
| C. | 元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共16个纵行 | |
| D. | X2+的核外有18个电子,则X在第四周期第ⅡA族 |
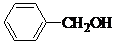 、
、 、
、 、
、 .
. .
.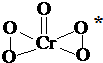 氧元素与多种元素具有亲和力,所形成化合物的种类很多.
氧元素与多种元素具有亲和力,所形成化合物的种类很多.