题目内容
16.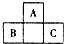 如图所示是元素周期表中短周期的一部分,已知B原子与C原子核外电子总数为A原子核外电子总数的4倍,则下列推断正确的是( )
如图所示是元素周期表中短周期的一部分,已知B原子与C原子核外电子总数为A原子核外电子总数的4倍,则下列推断正确的是( )| A. | A、B、C三者均为非金属元素 | B. | B与C只能形成一种共价化合物 | ||
| C. | A与B、A与C均可形成离子化合物 | D. | A、B、C三者最外层电子数之和为40 |
分析 由短周期元素在周期表中位置,可A处于第二周期,B、C处于第三周期,已知B原子与C原子核外电子总数之和为A的4倍,设A的原子序数x,则B的原子序数为x+7,C的原子序数为x+9,则x+7+x+9=4x,解得x=8,则A为O,B为P,C为Cl,以此来解答.
解答 解:由短周期元素在周期表中位置,可A处于第二周期,B、C处于第三周期,已知B原子与C原子核外电子总数之和为A的4倍,设A的原子序数x,则B的原子序数为x+7,C的原子序数为x+9,则x+7+x+9=4x,解得x=8,则A为O,B为P,C为Cl,
A.A为O元素,B为P元素,C为Cl元素,三种元素都是非金属,故A正确;
B.P与Cl可以形成PCl3、PCl5,故B错误;
C.P与O、O与Cl均可以形成共价化合物,故C错误;
D.A、B、C三者最外层电子数分别为6、5、7,之和为18,故D错误.
故选A.
点评 本题考查结构性质位置关系的应用,难度不大,推断元素是解题关键,注意理解同主族元素原子序数关系.

练习册系列答案
相关题目
6.下列关于分子或晶体中心原子的杂化类型的说法正确的是( )
| A. | CH3CH3中的两个碳原子与BF3中的硼原子均采取sp2杂化 | |
| B. | 晶体硅和石英晶体中的硅原子均采取sp3杂化 | |
| C. | BeCl2中的铍原子和H2O中的氧原子均采取sp杂化 | |
| D. | CO2中的碳原子与CH2=CH2中的两个碳原子均采取sp杂化 |
4.1mol H2表示的含义是( )
| A. | 1 mol 氢 | B. | 1 mol 氢气 | C. | 1 mol 氢分子 | D. | 1 mol 氢原子 |
1.下列颜色变化不是因为发生化学变化引起的是( )
| A. | 一氧化氮气体暴露空气中变成红棕色 | |
| B. | 盛放在无色试剂瓶中的浓硝酸呈黄色 | |
| C. | 苯滴加到溴水中,振荡后水层接近无色 | |
| D. | 二氧化硫通入品红溶液后溶液显无色 |
8.根据下列某些短周期元素中元素性质的有关句回答问题.
(1)元素②、④、⑦和⑩的电负性由大到小的顺序是F>Cl>Al>Na(填元素符号).
(2)元素⑤、⑥和⑦的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质有CCl4、PCl3(写化学式).
(3)元素⑦离子的结构示意图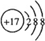 .
.
(4)元素①和⑨形成阳离子,其结构式为 ,其中心原子以sp3杂化轨道成键.
,其中心原子以sp3杂化轨道成键.
(5)元素②和⑦形成晶体的部分结构可用图中的A来表示.元素⑤最高价氧化物的晶体结构可以用下图C来表示.(填序号)
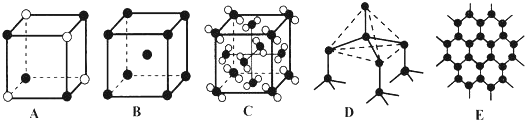
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |
| 原子半径/10 -10m | 0.37 | 1.86 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.52 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | +3 | +4 | +5 | +7 | +1 | +5 | ||
| 最低价态 | -1 | -2 | -4 | -3 | -1 | -3 | -1 |
(2)元素⑤、⑥和⑦的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质有CCl4、PCl3(写化学式).
(3)元素⑦离子的结构示意图
 .
.(4)元素①和⑨形成阳离子,其结构式为
 ,其中心原子以sp3杂化轨道成键.
,其中心原子以sp3杂化轨道成键.(5)元素②和⑦形成晶体的部分结构可用图中的A来表示.元素⑤最高价氧化物的晶体结构可以用下图C来表示.(填序号)

9.已知:
C(s)+O2(g)═CO2(g)△H1
CO2 (g)+C(s)═2CO(g)△H2
2CO (g)+O2(g)═2CO2(g)△H3
2Cu(s)+O2(g)═2CuO(s)△H4
CO(g)+CuO(s)═CO2(g)+Cu(s)△H5
下列关于上述反应焓变的判断正确的是( )
C(s)+O2(g)═CO2(g)△H1
CO2 (g)+C(s)═2CO(g)△H2
2CO (g)+O2(g)═2CO2(g)△H3
2Cu(s)+O2(g)═2CuO(s)△H4
CO(g)+CuO(s)═CO2(g)+Cu(s)△H5
下列关于上述反应焓变的判断正确的是( )
| A. | △H1>O,△H3<0 | B. | △H2<0,△H4>0 | C. | △H2=△H1-△H3 | D. | △H3=△H4+△H1 |

 .
.
 .
.