题目内容
1.如图,C、D、E、F、X、Y都是惰性电极.将电源接通后,向(乙)中滴入酚酞溶液,在 F极附近显红色.则下列说法正确的是( )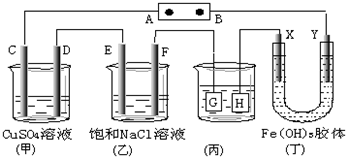
| A. | 若用乙烷、空气燃料电池作电源,电解质为KOH溶液,则B极的电极反应式为:O2+2H2O+4e-═4OH- | |
| B. | 欲用(丙)装置给铜镀银,H应该是Ag,电镀液是AgNO3溶液 | |
| C. | (丁)装置中Y极附近红褐色变深,说明氢氧化铁胶粒带正电荷 | |
| D. | C、D、E、F电极均有单质生成,其物质的量比为1:1:2:2 |
分析 C、D、E、F、X、Y都是惰性电极.将电源接通后,向(乙)中滴入酚酞溶液,在 F极附近显红色,F电极附近有NaOH生成,则F电极是阴极,CEGX都是阳极,DFHY都是阴极,所以A是正极、B是负极,
A.若用乙烷、空气燃料电池作电源,电解质为KOH溶液,通入乙烷的电极是负极、通入空气的电极是正极,阴极上乙烷失电子和氢氧根离子反应生成碳酸根离子和水;
B.若给Cu上镀Ag,镀层作阳极,镀件作阴极;
C.电解时,电解质中带正电荷的微粒向阴极移动,带负电荷是微粒向阳极移动;
D.C上是OH-放电、D上是Cu2+放电、E上是Cl-放电、F上是H+放电,根据转移电子守恒计算生成物质的物质的量之比.
解答 解:C、D、E、F、X、Y都是惰性电极.将电源接通后,向(乙)中滴入酚酞溶液,在 F极附近显红色,F电极附近有NaOH生成,则F电极是阴极,CEGX都是阳极,DFHY都是阴极,所以A是正极、B是负极,
A.燃料电池中,正极上氧化剂得电子发生还原反应,电极反应为O2+4e-+2H2O=4OH-,故A错误;
B.电镀时,镀层作阳极、镀件作阴极,则欲用(丙)装置给铜镀银,H应该是Cu、G是银,电镀液选是AgNO3溶液,故B错误;
C.带正电荷的胶粒向阴极移动,(丁)装置中Y极附近红褐色变深,说明氢氧化铁胶体粒子带正电荷,胶体不带电,故C正确;
D.C、D、E、F电极反应式分别为4OH--4e-=O2↑+2H2O、Cu2++2e-=Cu、2Cl--2e-=Cl2↑、2H++2e-=H2↑,当转移电子相等时,生成单质的物质的量之比为1:2:2:2,故D错误;
故选C.
点评 本题考查电解原理,为高频考点,正确判断正负极阴阳极是分解本题关键,难点是电极反应式的书写及D选项的计算,要结合电解质溶液酸碱性书写电极反应式,D中要明确串联电路中存在的转移电子守恒,题目难度不大.

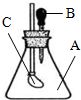 如图所示,锥形瓶内装有干燥的气体A,胶头滴管内盛有液体B,若挤压胶头滴管,使液体B滴入瓶中,振荡,一会儿可见小气球C鼓起.则对于气体A和液体B最可能的是( )
如图所示,锥形瓶内装有干燥的气体A,胶头滴管内盛有液体B,若挤压胶头滴管,使液体B滴入瓶中,振荡,一会儿可见小气球C鼓起.则对于气体A和液体B最可能的是( )| A. | A是Cl2,B是饱和NaCl溶液 | B. | A是NH3,B是酚酞溶液 | ||
| C. | A是H2,B是水 | D. | A是CO2,B是NaHCO3饱和溶液 |
| A. | 因为SO2具有漂白性,所以它能使品红溶液、溴水、酸性高锰酸钾溶液、石蕊试液褪色 | |
| B. | 能使品红溶液褪色的不一定是SO2 | |
| C. | SO2、漂白粉、活性炭、Na2O2都能使红墨水褪色,其原理相同 | |
| D. | SO2和Cl2等物质的量混合后通入装有湿润的有色布条的集气瓶中,漂白效果更好 |
SiCl4(g)+2Zn(l)?Si(s)+2ZnCl2(g)△H1
SiCl4(g)+2Zn(g)?Si(s)+2ZnCl2(g)△H2
下列说法正确的是( )
| A. | Zn(l)=Zn(g)△H=$\frac{1}{2}$(△H1-△H2) | |
| B. | 用硅制作的太阳能电池是将化学能转化为电能 | |
| C. | 增加 Zn(g)的量,△H2变大 | |
| D. | Zn-Cu-CuSO4溶液构成的原电池中,Cu片质量增加,Zn片质量不变 |
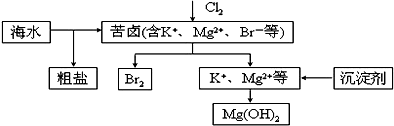 氯气在实验室和生产中都有重要的应用.
氯气在实验室和生产中都有重要的应用.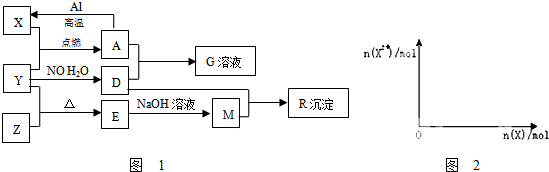
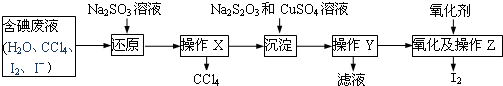
 ;
;
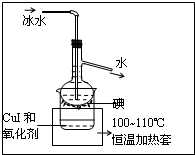
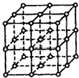 如图所示,直线交点处的圆圈为NaCl晶体中Na+离子或Cl-离子所处的位置.这两种离子在空间三个互相垂直的方向上都是等距离排列的.
如图所示,直线交点处的圆圈为NaCl晶体中Na+离子或Cl-离子所处的位置.这两种离子在空间三个互相垂直的方向上都是等距离排列的.