题目内容
当下列反应达到平衡时,保持温度不变,向容器中充入氩气,平衡一定不移动的是( )
| A、.2HI(g)═H2(g)+I2(g) |
| B、N2(g)+3H2(g)═2NH3(g) |
| C、PCl5(g)═PCl3(g)+Cl2(g) |
| D、2SO2(g)+O2(g)═2SO3(g) |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:当反应达到平衡时,保持温度不变,向容器中通入氩气,容器的体积可能为定值、可能增大,平衡一定不移动,说明反应前后气体的体积不发生变化.
解答:
解:当反应达到平衡时,保持温度不变,向容器中通入氩气,容器的体积可能为定值、可能增大,平衡一定不移动,说明反应前后气体的体积不发生变化,选项BCD中各反应前后气体的体积发生变化,A选项中反应前后气体的体积不发生变化,故选A.
点评:本题考查了压强对化学平衡的影响,注意应前后气体体积不变的化学反应,压强对其化学平衡不影响,为易错点.

练习册系列答案
相关题目
水由于受到有机物污染而造成富营养化,使水中鱼类大批死亡,鱼类死亡是因为( )
| A、藻类大量繁殖,抢走了鱼类的营养 |
| B、水中缺氧,窒息而死 |
| C、水中氧气过多 |
| D、水中含有有毒的金属元素过多 |
实验室进行中和热测定的实验时除需要大烧杯(500mL)、小烧杯(100mL)外,所用的其他仪器和试剂均正确的一组是( )
| A、0.50 mol?L-1盐酸,0.50 mol?L-1NaOH溶液,100 mL量筒1个 |
| B、0.50 mol?L-1盐酸,0.55 mol?L-1NaOH溶液,100 mL量筒2个 |
| C、0.50 mol?L-1盐酸,0.55 mol?L-1NaOH溶液,50 mL量筒1个 |
| D、0.50 mol?L-1盐酸,0.55 mol?L-1NaOH溶液,50 mL量筒2个 |
下列根据实验现象所得出的结论中,正确的是( )
| A、某物质焰色反应呈黄色,结论:该物质是钠盐 |
| B、无色试液加入NaOH溶液,加热产生的气体使红色石蕊试纸变蓝,结论:试液中含NH3 |
| C、无色溶液中加入BaCl2溶液有白色沉淀产生,再加盐酸,沉淀不消失,结论:原溶液一定含有SO42- |
| D、无色溶液中加入稀盐酸产生无色无味气体,该气体能使澄清石灰水变浑浊,结论:原溶液可能含有CO32- |
橙花醇具有玫瑰及苹果香气,可作为香料,其结构简式如图,下列关于橙花醇的叙述,错误的是( )
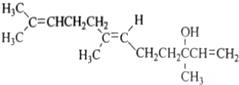

| A、分子式为C15H26O |
| B、既能发生取代反应,也能发生加成反应 |
| C、1mo1橙花醇在氧气中充分燃烧,需消耗470.4L氧气(标准状况) |
| D、1mo1橙花醇在室温下与溴四氯化碳溶液反应,最多消耗240g溴 |
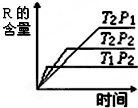 在密闭容器中进行下列反应:M(g)+N(g)R(g)+2L,反应符合右图.下列叙述正确的是( )
在密闭容器中进行下列反应:M(g)+N(g)R(g)+2L,反应符合右图.下列叙述正确的是( )| A、T2>T1,正反应放热,L是液体 |
| B、P2<P1,正反应吸热,L是固体 |
| C、T2<T1,正反应放热,L是气体 |
| D、P2>P1,正反应吸热,L是气体 |
把2.27gNaHCO3和Na2CO3?10H2O组成的混合物溶于水配成100ml溶液,其中C(Na+)=0.2mol?L-1,若将等质量的该混合物加热至恒重,所得固体质量为( )
| A、0.84g |
| B、1.06g |
| C、1.43g |
| D、2.27g |
下列有关溶液中粒子浓度的关系式中,正确的是( )
| A、pH相同的①CH3COONa ②NaHCO3 ③NaAlO2三份溶液中的c(Na+):③>②>① |
| B、0.1mol?L-1某二元弱酸强碱盐NaHA溶液中:c(Na+)=2c(A2-)+c(HA-)+c(H2A) |
| C、如图中a点溶液中各离子浓度的关系是:c(OH-)=c(H+)+c(CH3COO-)+2c(CH3COOH) |
D、如图中pH=7时:c(Na+)>c(CH3COO-)>c(OH-)=c(H+)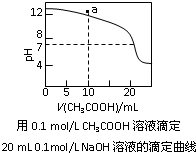 |