题目内容
 在密闭容器中进行下列反应:M(g)+N(g)R(g)+2L,反应符合右图.下列叙述正确的是( )
在密闭容器中进行下列反应:M(g)+N(g)R(g)+2L,反应符合右图.下列叙述正确的是( )| A、T2>T1,正反应放热,L是液体 |
| B、P2<P1,正反应吸热,L是固体 |
| C、T2<T1,正反应放热,L是气体 |
| D、P2>P1,正反应吸热,L是气体 |
考点:化学平衡的影响因素
专题:化学平衡专题
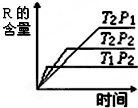
分析:由图象可知,温度为T2时,根据到达平衡的时间可知P2>P1,且压强越大,R的含量越低,说明平衡向逆反应方向移动,正反应为气体体积增大的反应;
压强为P2时,根据到达平衡的时间可知T1>T2,且温度越高,R的含量越低,说明平衡向逆反应方向移动,则正反应为放热反应.
压强为P2时,根据到达平衡的时间可知T1>T2,且温度越高,R的含量越低,说明平衡向逆反应方向移动,则正反应为放热反应.
解答:
解:由图象可知,温度为T2时,根据到达平衡的时间可知P2>P1,且压强越大,R的含量越低,说明平衡向逆反应方向移动,正反应为气体体积增大的反应,故L为气体;
压强为P2时,根据到达平衡的时间可知T1>T2,且温度越高,R的含量越低,说明平衡向逆反应方向移动,则正反应为放热反应;
由上述分析可知,该反应的正反应为放热反应,L是气体,
故选C.
压强为P2时,根据到达平衡的时间可知T1>T2,且温度越高,R的含量越低,说明平衡向逆反应方向移动,则正反应为放热反应;
由上述分析可知,该反应的正反应为放热反应,L是气体,
故选C.
点评:本题考查化学平衡图象问题,难度不大,本题注意根据图象判断温度、压强的大小,根据温度、压强对平衡移动的影响分析.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
120℃和101kPa时,乙烷、乙炔和丙烯组成的混合烃1L与9L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是10L,原混合烃中乙炔的体积分数为( )
| A、12.5% | B、25% |
| C、50% | D、75% |
某工业废水含有下列离子中的5种(不考虑水的电离及离子的水解),K+、Cu2+、Al3+、Fe2+、Cl-、CO32-、NO3-、SO42-,且各种离子的物质的量浓度相等.甲同学欲探究废水的组成,进行了如下实验:
①用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃观察有紫色火焰.
②另取溶液加入足量稀盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变.
③另取溶液加入BaCl2溶液,有白色沉淀生成.
根据上述实验,以下推测正确的是( )
①用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃观察有紫色火焰.
②另取溶液加入足量稀盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变.
③另取溶液加入BaCl2溶液,有白色沉淀生成.
根据上述实验,以下推测正确的是( )
| A、溶液中难以确定Cl-的存在与否 |
| B、原溶液中所含的离子为:Fe2+、K+、NO3-、SO42- |
| C、步骤②中可以确定Fe2+、NO3-的存在,不能确定其它离子是否存在 |
| D、步骤③中的白色沉淀为2种钡盐 |
当下列反应达到平衡时,保持温度不变,向容器中充入氩气,平衡一定不移动的是( )
| A、.2HI(g)═H2(g)+I2(g) |
| B、N2(g)+3H2(g)═2NH3(g) |
| C、PCl5(g)═PCl3(g)+Cl2(g) |
| D、2SO2(g)+O2(g)═2SO3(g) |
镁锌合金粉末7.7g恰好与一定质量20%的稀硫酸完全反应,将反应后的溶液蒸发,经处理后得到不含结晶水的固体22.1g,则反应中生成氢气的质量为( )
| A、0.1g | B、0.2g |
| C、0.3g | D、0.4g |
自全面建设小康社会以来,人们的生活水平逐年提高,更注重身体健康和食品卫生.下列做法会导致食品对人体健康有害的是( )
| A、烹饪时使用加铁酱油 |
| B、在食盐中添加适量碘元素 |
| C、多吃新鲜蔬菜 |
| D、用硫磺(S)熏蒸漂白银耳 |