题目内容
3.今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Ca2+、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:第一份加入AgNO3溶液有沉淀产生;
第二份加入足量NaOH溶液加热后,收集到0.08mol气体;
第三份加入足量BaCl2 溶液后,得到干燥沉淀12.54g,经足量的盐酸洗涤、干燥后,沉淀质量为4.66g.
根据上述实验,回答以下问题:
(1)由第一份进行的实验推断该混合物是否一定含有Cl-否,
(2)由第二份进行的实验可知混合物中应含NH4+离子,其物质的量浓度为0.8mol/L.
(3)由第三份进行的实验可知12.54g 沉淀的成份为BaCO3、BaSO4.请计算形成该沉淀的原混合物中各离子的物质的量n(CO32-)=0.04mol、n(SO42-)=0.02mol.
(4)综合上述实验,你认为以下结论正确的是A
A.该混合物中一定含有K+、NH4+、CO32-、SO42-,可能含有Cl-,且n(K+)≥0.04mol
B.该混合物中一定含有NH4+、CO32-、SO42-,可能含有Ca2+、K+、Cl-
C.该混合物中一定含有NH4+、CO32-、SO42-,可能含有K+、Cl-
D.该混合物中一定含有NH4+、SO42-,可能含有Ca2+、K+、Cl-.
分析 ①加入AgNO3溶液有沉淀产生,说明溶液中可能存在Cl-、CO32-、SO42-;
②0.08mol气体为氨气,溶液中一定含有NH4+,并且物质的量为0.08mol;
③4.66g沉淀为硫酸钡,12.54g沉淀为硫酸钡和碳酸钡的混合物;
再根据电荷守恒,得出一定存在钾离子,据此进行解答.
解答 解:①第一份加入AgNO3溶液有沉淀产生,与AgNO3溶液有沉淀产生的离子有:Cl-、CO32-、SO42-;
②加足量NaOH溶液加热产生气体,气体是氨气,故一定有铵离子0.04mol,溶液中一定含有NH4+,并且物质的量为0.04mol;
③不溶于盐酸的4.66g为硫酸钡,物质的量为:$\frac{4.66g}{233g/mol}$=0.02mol;12.54g沉淀是硫酸钡和碳酸钡,碳酸钡质量为12.54g-4.66g=7.88g,碳酸钡的物质的量为:$\frac{7.88g}{197g/mol}$=0.04mol,故原溶液中一定存在CO32-、SO42-,则一定没有Mg2+、Ba2+;
再根据电荷守恒,正电荷为:n(+)=n(NH4+)=0.08mol;c(-)=2c(CO32-)+2c(SO42-)=0.12mol,正电荷总物质的量大于负电荷,故原溶液中一定有K+,至少为0.04mol;
综合以上可以得出,一定存在的离子有:NH4+、K+、CO32-、SO42-,一定没有的离子Mg2+、Ba2+,可能存在Cl-;
(1)由第一份进行的实验推断该混合物是否一定含有Cl-,不能,因为生成碳酸银和硫酸银也有白色沉淀,故答案为:否;
(2)由第二份进行的实验可知混合物中应含NH4+,其物质的量为0.08mol,浓度为0.08mol÷0.1L=0.8 mol/L;
(3)不溶于盐酸的4.66g为硫酸钡,物质的量为:$\frac{4.66g}{233g/mol}$=0.02mol,可知溶液里n(SO42-)=0.02mol;12.54g沉淀是硫酸钡和碳酸钡,碳酸钡质量为12.54g-4.66g=7.88g,碳酸钡的物质的量为:$\frac{7.88g}{197g/mol}$=0.04mol,可知溶液里n (CO32-)=0.04mol,故答案为:BaCO3、BaSO4;n (CO32-)=0.04mol、n(SO42-)=0.02mol;
(4)结合分析可知原溶液里一定存在的离子有:NH4+、K+、CO32-、SO42-,一定没有的离子Mg2+、Ba2+,可能存在Cl-,再根据电荷守恒,正电荷为:n(+)=n(NH4+)=0.08mol;c(-)=2c(CO32-)+2c(SO42-)=0.12mol,正电荷总物质的量大于负电荷,故原溶液中一定有K+,至少为0.04mol,选项A正确,故答案为:A.
点评 本题考查常见阴、阳离子的检验方法,题目难度中等,注意掌握常见离子的化学性质及检验方法,本题中根据电荷守恒判断钾离子的存在为易错点,做题时需要细致分析.

| A. | M只能是碱类 | B. | M只能是盐类 | C. | M一定为电解质 | D. | M可能为非电解质 |
| A. | 浓硫酸具有吸水性,因而能使蔗糖炭化 | |
| B. | 浓硫酸在常温下不容易与铜片反应放出二氧化硫气体 | |
| C. | 浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体 | |
| D. | 浓硫酸在常温下能够使铁、铝、锌等金属钝化 |
| A. | 燃料电池只能在燃烧的情况下才能发生 | |
| B. | 燃料电池是将化学能转化为电能的装置 | |
| C. | 燃料电池属于二次电池的一种 | |
| D. | 燃料电池与燃料燃烧时对能量的转化率完全相同 |
| 物质 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 1.8 | 6.3 | 5.2 |
| 完全沉淀的pH | 3.0 | 8.3 | 6.7 |
实验步骤:
Ⅰ.取一定量样品于烧杯中,加足量NaOH溶液,有气体产生,过滤得固体A和无色溶液B;
Ⅱ.向B中加入稀硫酸,出现白色沉淀,继续滴加稀硫酸至过量,白色沉淀完全溶解;
Ⅲ.向A中加入足量稀硫酸并微热,固体完全溶解,得溶液C;
Ⅳ.向C中加入NaClO,调节溶液的pH至4~5,产生红褐色沉淀,过滤得到蓝绿色溶液D;
Ⅴ.向D中加入NaOH,调节溶液的pH到7~8,产生蓝色絮状沉淀. 请回答下列问题.
(1)Ⅰ中产生气体的离子方程式为2Al+2OH-+2H2O═2AlO2-+3H2↑.
(2)由Ⅰ、Ⅱ知,原样品中一定不存在的物质是SiO2.
(3)溶液C中除H+、Cu2+外一定还含有的阳离子是Fe2+;为验证溶液C中存在该阳离子,可选用的试剂及对应的现象是向酸性KMnO4溶液中滴加待测液,褪色.
(4)Ⅳ中加NaClO的目的是将Fe2+氧化成Fe3+,增大溶液的pH使Fe3+生成Fe(OH)3沉淀.
(5)由上述实验可以获得结论:原样品所有可能的成分组合为组合1:Al、Fe2O3、Cu2O;组合2:Al、Cu2O、Fe3O4(Al、Fe2O3、Cu2O、Fe3O4); …(用化学式表示,空不够可以补充.)
| A. | 水晶 | B. | 有色玻璃 | C. | 青花瓷 | D. | 水泥 |
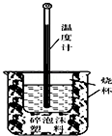 某学习小组的同学在实验室利用如图装置进行中和热的测定.回答下列问题:
某学习小组的同学在实验室利用如图装置进行中和热的测定.回答下列问题: