题目内容
18.设NA表示阿伏加德罗常数,下列说法中正确的是( )| A. | NA个N2分子和NA个CO分子质量比为1:2 | |
| B. | 1 mol H2O的质量等于NA个H2O质量的总和 | |
| C. | 在任何条件下1mol H2所含的原子数为NA | |
| D. | 1mol H2SO4中所含的粒子数目一定是NA |
分析 A.氮气和一氧化碳的摩尔质量相同,分子数相同时二者物质的量相等,根据m=nM可知二者质量相等;
B.1mol水分子含有NA个H2O;
C.1mol氢气分子中含有2mol氢原子;
D.题中没有指明粒子的种类.
解答 解:A.NA个N2分子和NA个CO分子的物质的量相等,二者摩尔质量都是28g/mol,则二者质量比为1:1,故A错误;
B.1 mol H2O的质量为18g,NA个H2O质量也是18g,二者质量相等,故B正确;
C.1mol H2含有2molH原子,含有的原子数为2NA,故C错误;
D.1mol H2SO4中所含的粒子数目,没有指明粒子的种类,无法计算粒子数目,故D错误;
故选B.
点评 本题考查物质的量的计算,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
9.高聚物••--CH2-CH2-CH2-是用下列何种物质聚合而成的( )
| A. | CH3-CH3 | B. | CH3-CH2-CH3 | C. | CH2=CH-CH3 | D. | CH2=CH2 |
6.两种金属混合物粉末16g,与足量的盐酸反应时生成标准状况下11.2L氢气,符合上述情况的金属混合物是( )
| A. | Mg,Fe | B. | Zn,Ag | C. | Fe,Zn | D. | Mg,Al |
13.下列关于“剂”的说法正确的是( )
| A. | 卤制品中可添加亚硝酸盐作为增色剂 | |
| B. | 补血剂口服液中添加的维生素C作为氧化剂 | |
| C. | 中国古代用明矾溶液做铜镜表面铜锈的除锈剂 | |
| D. | 月饼包装盒内放有小袋铁粉主要作为干燥剂 |
3.已知 X2(g)+Y2 (g)?2Z(g),X2、Y2、Z 的起始浓度分别为 0,1mol•L-1、0.3mol•L-1,0.2mol•L-1.在一定条件下,当反应达到平衡时,各物质的浓度可能是( )
| A. | Z 为 0.4mol•L-1 | B. | X 为 0.2 mol•L-1 | ||
| C. | Y 为 0.4 mol•L-1 | D. | Z 为 0.3 mol•L-1 |
10. 已知 25℃时部分弱电解质的电离平衡常数数据如表:
已知 25℃时部分弱电解质的电离平衡常数数据如表:
回答下列问题:
(1)写出碳酸的主要的电离方程式H2CO3?H++HCO3-.若将碳酸饱和溶液稀释 10 倍,则稀释后的溶液中 c(H+)大于原来的十分之一(填“大于”、“小于”或“等于”).
(2)物质的量浓度均为 0.1mol/L 的五种溶液:pH 由小到大的顺序为e<a<d<c<b(用编号填写).
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3 e.NaSCN
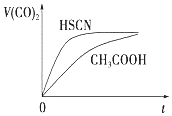
(3)25℃时,将 20mL0.1mol•L-1CH COOH 溶液和 20mL0.1mol•L-1HSCN 溶液分别与 20mL0.1mol•L-1NaHCO 溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图.反应初始阶段两种溶液产生 CO2气体的速率存在明显差异的原因是HSCN的酸性比CH3COOH强,其溶液中c(H+)较大,故其溶液与NaHCO3溶液的反应速率快反应结束后,假设 NaHCO3完全反应且气体全部逸出,则所得两溶液中,c(CH3COO)<c(SCN)(填“>”、“<”或“=”)
(4)25℃时,CH3COONa 与 CH3COOH 的混合溶液,若测得 pH=8,则溶液中c(Na+)-c(CH3COO-)=10-6-10-8mol/L(填代入数据后的计算式,不必算出具体数值).
(5)向 NaClO 溶液中通入少量的 CO2,发生反应的离子方程式为ClO-+CO2+H2O═HClO+HCO3-.
 已知 25℃时部分弱电解质的电离平衡常数数据如表:
已知 25℃时部分弱电解质的电离平衡常数数据如表:| 化学式 | HSCN | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.3×10-1 | 1.8×10-5 | Ka1=4.3×10-1Ka2=5.6×10-1 | 3.0×10-8 |
(1)写出碳酸的主要的电离方程式H2CO3?H++HCO3-.若将碳酸饱和溶液稀释 10 倍,则稀释后的溶液中 c(H+)大于原来的十分之一(填“大于”、“小于”或“等于”).
(2)物质的量浓度均为 0.1mol/L 的五种溶液:pH 由小到大的顺序为e<a<d<c<b(用编号填写).
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3 e.NaSCN
(3)25℃时,将 20mL0.1mol•L-1CH COOH 溶液和 20mL0.1mol•L-1HSCN 溶液分别与 20mL0.1mol•L-1NaHCO 溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图.反应初始阶段两种溶液产生 CO2气体的速率存在明显差异的原因是HSCN的酸性比CH3COOH强,其溶液中c(H+)较大,故其溶液与NaHCO3溶液的反应速率快反应结束后,假设 NaHCO3完全反应且气体全部逸出,则所得两溶液中,c(CH3COO)<c(SCN)(填“>”、“<”或“=”)
(4)25℃时,CH3COONa 与 CH3COOH 的混合溶液,若测得 pH=8,则溶液中c(Na+)-c(CH3COO-)=10-6-10-8mol/L(填代入数据后的计算式,不必算出具体数值).
(5)向 NaClO 溶液中通入少量的 CO2,发生反应的离子方程式为ClO-+CO2+H2O═HClO+HCO3-.
7.在由C2H4,C3H6和CH2O组成的混合气体中,碳元素的质量分数是60%,则该混合气体中氧元素的质量分数为( )
| A. | 30% | B. | 10% | C. | 20% | D. | 24% |
 ,X2Y属于共价化合物(填离子化合物、共价化合物、共价分子);
,X2Y属于共价化合物(填离子化合物、共价化合物、共价分子);