题目内容
7.在由C2H4,C3H6和CH2O组成的混合气体中,碳元素的质量分数是60%,则该混合气体中氧元素的质量分数为( )| A. | 30% | B. | 10% | C. | 20% | D. | 24% |
分析 根据在C2H4,C3H6和CH2O混合物中,C原子与H原子数目之比是定值,为1:2,故m(C):m(H)=12:2=6:1,根据碳元素的质量分数求出氢元素的质量分数,进而求出氧元素的质量分数,据此解答.
解答 解:在由C2H4,C3H6和CH2O组成的混合气体中,只有3种元素C、H、O,C原子与H原子数目之比是定值,为1:2,故m(C):m(H)=12:2=6:1,碳元素的质量分数为60%,则氢元素的质量分数为10%,O的质量分数为1-60%-10%=30%.
故选A.
点评 本题考查质量分数的有关计算,根据分子式判断C、H两元素的质量之比为定值是解题关键,题目难度中等,侧重于考查学生的分析能力和计算能力.

练习册系列答案
 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
17.下列图示与对应的叙述相符合的是( )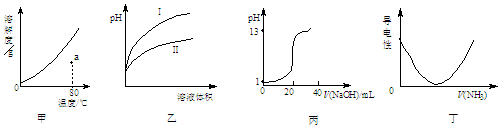

| A. | 图甲表示KNO3的溶解度曲线,a点所示溶液是80℃时KNO3的不饱和溶液 | |
| B. | 图乙表示用水稀释pH相同的盐酸和醋酸,I表示醋酸,II表示盐酸 | |
| C. | 图丙表示0.1000 mol•L-1NaOH溶液滴定20.00 mL 0.1000 mol•L-1CH3COOH溶液所得到的滴定曲线 | |
| D. | 图丁表示将NH3通入醋酸溶液的过程中,溶液导电性的变化 |
18.设NA表示阿伏加德罗常数,下列说法中正确的是( )
| A. | NA个N2分子和NA个CO分子质量比为1:2 | |
| B. | 1 mol H2O的质量等于NA个H2O质量的总和 | |
| C. | 在任何条件下1mol H2所含的原子数为NA | |
| D. | 1mol H2SO4中所含的粒子数目一定是NA |
15.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 1 mol FeCl3水解生成的 Fe(OH)3胶粒数为 lNA | |
| B. | 将 lmol Cl2通人水中,HC1O、Cl、C1O 粒子数之和为 2NA | |
| C. | 1 mol Fe 溶于过量硝酸,电子转移数为 2NA | |
| D. | 10℃时,lL pH=1.0 的 H2SO4溶液中含 H+为 0.1NA |
2.若某氖原子一个原子质量是a g,NA是阿伏加德罗常数的值,下列说法正确的是( )
| A. | 氖元素的相对原子质量是a | |
| B. | 该氖原子的摩尔质量是aNAg | |
| C. | Wg该氖原子的物质的量一定是$\frac{W}{{a{N_A}}}$mol | |
| D. | Wg该氖气的体积是22.4$\frac{W}{{a{N_A}}}$升 |
12.V L含有(NH4)2SO4和Al2(SO4)3的混合溶液,已知NH4+浓度为a mol•L-1;SO42-浓度为bmol•L-1.则原混合溶液中铝离子的物质的量浓度为( )
| A. | (b-2a)/3mol•L-1 | B. | (b-2a)/2mol•L-1 | C. | (2b-a)/3mol•L-1 | D. | (2b-a)/2 mol•L-1 |
16.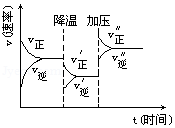 如图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )
如图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )
 如图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )
如图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )| A. | 正反应是吸热反应 | |
| B. | 若A、B是气体,则D是液体或固体 | |
| C. | 若A、B是气体,则C、D中至少有一种不是气体 | |
| D. | A、B、C、D均为气体 |
17.以下各种尾气吸收装置中,适合于吸收氯化氢气体的是( )
| A. |  | B. |  | C. |  | D. |  |