题目内容
4.某消毒液的主要成分为NaClO,还含有一定量的NaOH,常温下分别取该消毒液并向其中加入指定物质,反应后的溶液中主要存在的一组离子正确的是( )| A. | 通入过量SO2:H+、Cl-、ClO-、HSO3- | |
| B. | 通入过量FeSO4溶液:Fe2+、H+SO42-、ClO- | |
| C. | 加入少量Al2(SO4)3溶液:Al3+、H+、ClO-、SO42- | |
| D. | 加入少量Na2O2固体:Na+、Cl-、ClO-、OH- |
分析 A.二氧化硫可与HClO发生氧化还原反应;
B.酸性条件下,ClO-可氧化Fe2+;
C.H+、ClO-反应生成弱酸;
D.过氧化钠可与水反应生成氢氧化钠,溶液呈碱性.
解答 解:A.二氧化硫具有还原性,可与HClO发生氧化还原反应,ClO-、HSO3-不能大量共存,故A错误;
B.酸性条件下,ClO-可氧化Fe2+,不能大量共存,故B错误;
C.H+、ClO-反应生成弱酸,且ClO-与铝离子发生互促水解,故C错误;
D.过氧化钠可与水反应生成氢氧化钠,溶液呈碱性,碱性条件下,Na+、Cl-、ClO-、OH-不发生反应,可大量共存,故D正确.
故选D.
点评 本题考查了氧化还原反应、离子共存等知识,为高频考点,侧重于考查氧化还原反应以及物质氧化性的应用,题目难度中等,注意把握NaClO的性质.

练习册系列答案
相关题目
14.下列解释事实的方程式正确的是( )
| A. | 用CuCl2溶液做导电实验,灯泡发光:CuCl2 $\frac{\underline{\;电解\;}}{\;}$Cu2++2Cl- | |
| B. | 铅蓄电池放电时,负极增重:Pb-2e-+SO42-=PbSO4 | |
| C. | 向碳酸钠溶液中滴加酚酞时,溶液变红:CO32-+2H2O?H2CO3+2OH- | |
| D. | 明矾可用于净水:Al3++3H2O?Al(OH)3↓+3H+ |
15.如图烧杯中盛有海水,铁在其中被腐蚀由快到慢的顺序为( )
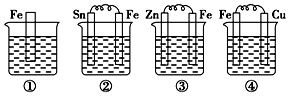

| A. | ②①③④ | B. | ④③②① | C. | ④②①③ | D. | ③②④① |
12.下列过程只涉及物理变化的是( )
| A. | 冰雪消融 | B. | 食物腐败 | C. | 钻木取火 | D. | 蜡炬成灰 |
19.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 使甲基橙变红的溶液:Na+、NH4+、SO32-、Cl- | |
| B. | $\frac{{K}_{W}}{c({H}^{+})}$=0.1mol/L的溶液:K+、Na+、SiO32-、CO32- | |
| C. | SO2的饱和溶液:Na+、K+、ClO-、SO42- | |
| D. | 由水电离产生的c(H+)=1×10-12 mol•L-1的溶液:Fe3+、K+、NO3-、SO42- |
9.日常生活中常用到加碘食盐和铁强化酱油,这里的碘和铁指的是( )
| A. | 元素 | B. | 单质 | C. | 原子 | D. | 分子 |
16.下列离子方程式中书写正确的是( )
| A. | FeCl2 溶液中通入Cl2:Fe2++Cl2═Fe3++2Cl- | |
| B. | 金属钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| C. | 稀硝酸和铜反应:Cu+2H+═Cu2++H2↑ | |
| D. | 稀盐酸与碳酸钙反应:2H++CaCO3═Ca2++H2O+CO2↑ |
13.下列各组离子在溶液中能大量共存的是( )
| A. | Cu2+、Mg2+、SO42-、NO3- | B. | H+、Mg2+、SO42-、HCO3- | ||
| C. | Ag+、Na+、NO3-、Cl- | D. | NH4+、Ba2+、NO3-、OH- |
9.下列各组离子在强酸性溶液中能大量共存的是( )
| A. | K+、Na+、HCO3-、SO42- | B. | Na+、Fe3+、I-、CI- | ||
| C. | Na+、NH4+、NO3-、CI- | D. | Na+、Ba2+、SO42-、NO3- |