题目内容
19.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )| A. | 使甲基橙变红的溶液:Na+、NH4+、SO32-、Cl- | |
| B. | $\frac{{K}_{W}}{c({H}^{+})}$=0.1mol/L的溶液:K+、Na+、SiO32-、CO32- | |
| C. | SO2的饱和溶液:Na+、K+、ClO-、SO42- | |
| D. | 由水电离产生的c(H+)=1×10-12 mol•L-1的溶液:Fe3+、K+、NO3-、SO42- |
分析 A.使甲基橙变红的溶液中存在大量氢离子,亚硫酸根离子与氢离子反应;
B.$\frac{{K}_{W}}{c({H}^{+})}$=0.1mol/L的溶液呈碱性,溶液中存在大量氢氧根离子,四种离子之间不反应,都不与氢氧根离子反应;
C.次氯酸根离子具有氧化性,能够氧化二氧化硫;
D.由水电离产生的c(H+)=1×10-12 mol•L-1的溶液呈酸性或碱性,铁离子与氢氧根离子反应.
解答 解:A.使甲基橙变红的溶液呈酸性,溶液中存在的氢离子,SO32-与氢离子反应,在溶液中不能大量共存,故A错误;
B.$\frac{{K}_{W}}{c({H}^{+})}$=0.1mol/L的溶液中存在大量氢氧根离子,K+、Na+、SiO32-、CO32-之间不发生反应,都不与氢氧根离子反应,在溶液中能够大量共存,故B正确;
C.SO2、ClO-之间发生氧化还原反应,在溶液中不能电离出,故C错误;
D.由水电离产生的c(H+)=1×10-12 mol•L-1的溶液中存在大量氢离子或氢氧根离子,Fe3+与氢氧根离子反应,在碱性溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.

练习册系列答案
相关题目
9.t℃时,在体积不变的密闭容器中发生反应:X(g)+3Y(g)?2Z(g),各组分在不同时刻的浓度如表:
下列说法正确的是( )
| 物质 | X | Y | Z |
| 初始浓度/(mol•L-1) | 0.1 | 0.2 | 0 |
| 2min末浓度/(mol•L-1) | 0.08 | a | b |
| 平衡浓度/(mol•L-1) | 0.05 | 0.05 | 0.1 |
| A. | 平衡时,X的转化率为5% | |
| B. | t℃时,该反应的平衡常数为40 | |
| C. | 增大平衡后的体系压强,v(正)增大,v(逆)减小,平衡向正反应方向移动 | |
| D. | 2 min内,用Y的变化量表示的平均反应速率v(Y)=0.03 mol•L-1•min-1 |
10.在实验室中,常用 KMnO4代替 MnO2与浓盐酸反应制取氯气,其反应的化学方程式为2KMnO4+16HCl(浓)=2MnCl2+5Cl2↑+2KCl+8H2O,下列叙述中正确的是( )
| A. | 反应中 KMnO4被氧化 | |
| B. | 氧化产物与还原产物的物质的量之比为 2:5 | |
| C. | 每生成 1 mol Cl2时,反应中转移的电子为 2 mol | |
| D. | 每消耗 16 molHCl 时,其中作氧化剂的 HCl 是 10 mol |
7.以下物质间的转化通过一步反应不能实现的是( )
| A. | NH3→NO2 | B. | C→CO2 | C. | Na2O2→Na2CO3 | D. | S→SO2 |
14.关于反应方程式Al2O3+N2+3C$\frac{\underline{\;高温\;}}{\;}$2AlN+3CO下列叙述正确的是( )
| A. | C是氧化剂 | B. | N2被还原 | ||
| C. | Al2O3发生氧化反应 | D. | 生成1 mol AlN转移6 mol电子 |
4.某消毒液的主要成分为NaClO,还含有一定量的NaOH,常温下分别取该消毒液并向其中加入指定物质,反应后的溶液中主要存在的一组离子正确的是( )
| A. | 通入过量SO2:H+、Cl-、ClO-、HSO3- | |
| B. | 通入过量FeSO4溶液:Fe2+、H+SO42-、ClO- | |
| C. | 加入少量Al2(SO4)3溶液:Al3+、H+、ClO-、SO42- | |
| D. | 加入少量Na2O2固体:Na+、Cl-、ClO-、OH- |
11.下列物质中,既能够导电又属于电解质的是( )
| A. | 固体氯化钠 | B. | 熔融氯化镁 | C. | 氯化氢气体 | D. | 氨水 |
8.常温下,下列说法不正确的是( )
| A. | 0.2 mol•L-1的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(OH-)>c(H+) | |
| B. | 0.02mol/L的NaOH溶液与0.04mol/L的NaHC2O4溶液等体积混合液:2c(OH-)+c(C2O42-)=c(HC2O4)+2c(H+) | |
| C. | 叠氨酸(NH3)与醋酸酸性相近,0.1mol•L-1 NaN3水溶液中离子浓度大小顺序为:c(Na+)>c(N3-)>c(OH-)>c(H+) | |
| D. | 向氨水中逐滴滴入盐酸至溶液的pH=7,则混合液中:c(NH4+)=c(Cl-) |
4.杀鼠灵是一种抗凝血性杀毒剂,其结构简式如图,下列说法正确的是( )
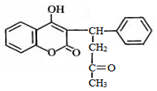

| A. | 分子中有1个手性碳原子 | B. | 遇FeCl3溶液显紫色 | ||
| C. | 1mol杀鼠灵最多能与9molH2反应 | D. | 能发生加成、取代、氧化反应 |