题目内容
7.有人欲配制下列含有四种不同阴、阳离子的溶液,其中能配制成功的是( )| A. | K+、H+、SO42-、CO32- | B. | Na+、Ca2+、SO42-、NO3- | ||
| C. | Ag+、Mg2+、Cl-、S2- | D. | Na+、Cu2+、Cl-、SO42- |
分析 A.氢离子与碳酸根离子反应;
B.钙离子与硫酸根离子反应生成硫酸钙沉淀;
C.银离子、镁离子与硫离子发生反应;
D.四种离子之间不发生反应,能够配制成功.
解答 解:A.H+、CO32-之间发生反应,不能大量共存,则无法配制该溶液,故A错误;
B.Ca2+、SO42-之间反应生成硫酸钙沉淀,不能大量共存,所以无法配制该溶液,故B错误;
C.Ag+、Mg2+与S2-之间发生反应,在溶液中不能大量共存,则无法配制该溶液,故C错误;
D.Na+、Cu2+、Cl-、SO42-之间不发生反应,可以大量共存,故能够配制该溶液,故D正确;
故选D.
点评 本题以配制溶液为载体考查了离子共存,为高考热点内容,熟悉离子共存的条件及物质的性质是解本题关键,注意隐含条件的挖掘,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案
相关题目
15.利用相似相溶原理不能解释的是( )
| A. | I2微溶于水,易溶于CCl4;HCl易溶于水 | |
| B. | 在水中的溶解度:C2H5OH>CH3CH2CH2CH2OH | |
| C. | 不同的烃之间相互溶解 | |
| D. | I2易溶于KI溶液中 |
2.钾长石的主要成分为硅酸盐,由前20号元素中的四种组成,化学式为XYZ3W8,其中只有W显负价.X、Y的最外层电子数之和与Z的最高正价数相等,Y3+与W的阴离子具有相同的电子层结构,X、W的质子数之和等于Y、Z的质子数之和.下列说法错误的是( )
| A. | X的离子半径>Y的离子半径 | |
| B. | Z的氢化物稳定性>W的氢化物稳定性 | |
| C. | 化合物X2W2和Y2W3中都不含配位键 | |
| D. | 1 mol ZW2晶体所含Z-W键的数目为4NA |
16.从结构上分析,有一种物质不同于其他三种,该物质是( )
| A. | 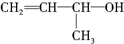 | B. | CH2═CH-CH3 | C. | 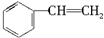 | D. | 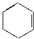 |
10.ZrO2常用作陶瓷材料,可由锆英砂(主要成分为ZrSiO4,也可表示为ZrO2•SiO2,还含少量Fe2O3、Al2O3、SiO2等杂质)通过如图方法制取.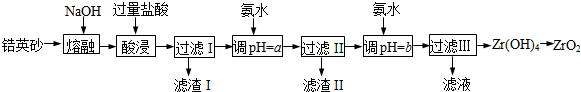
已知:①ZrO2能与烧碱反应生成可溶于水的Na2ZrO3,Na2ZrO3与酸反应生成ZrO2+.
②部分金属离子在实验条件下开始沉淀和完全沉淀的pH如表.
(1)熔融时ZrSiO4发生反应的化学方程式为ZrSiO4+4NaOH $\frac{\underline{\;高温\;}}{\;}$Na2SiO3+Na2ZrO3+2H2O,滤渣I的化学式为H2SiO3.
(2)为使滤液I的杂质离子沉淀完全,需用氨水调pH=a,则a的范围是5.2~6.2;继续加氨水至pH=b时,所发生反应的离子方程式为ZrO2++2NH3•H2O+H2O=Zr(OH)4↓+2NH4+.
(3)向过滤Ⅲ所得滤液中加入CaCO3粉末并加热,得到两种气体.该反应的离子方程式为2NH4++CaCO3=Ca2++2NH3↑+CO2↑+H2O.
(4)为得到纯净的ZrO2,Zr(OH)4需要洗涤,检验Zr(OH)4是否洗涤干净的方法是取最后一次洗涤液,向其中滴加稀硝酸,再滴加硝酸银溶液,若无沉淀生成,则Zr(OH)4洗涤干净.

已知:①ZrO2能与烧碱反应生成可溶于水的Na2ZrO3,Na2ZrO3与酸反应生成ZrO2+.
②部分金属离子在实验条件下开始沉淀和完全沉淀的pH如表.
| 金属离子 | Fe3+ | Al3+ | ZrO2+ |
| 开始沉淀时pH | 1.9 | 3.3 | 6.2 |
| 沉淀完全时pH | 3.2 | 5.2 | 8.0 |
(2)为使滤液I的杂质离子沉淀完全,需用氨水调pH=a,则a的范围是5.2~6.2;继续加氨水至pH=b时,所发生反应的离子方程式为ZrO2++2NH3•H2O+H2O=Zr(OH)4↓+2NH4+.
(3)向过滤Ⅲ所得滤液中加入CaCO3粉末并加热,得到两种气体.该反应的离子方程式为2NH4++CaCO3=Ca2++2NH3↑+CO2↑+H2O.
(4)为得到纯净的ZrO2,Zr(OH)4需要洗涤,检验Zr(OH)4是否洗涤干净的方法是取最后一次洗涤液,向其中滴加稀硝酸,再滴加硝酸银溶液,若无沉淀生成,则Zr(OH)4洗涤干净.
 CH3COOCH2CH3+H2O.该反应类型是酯化(取代)反应.
CH3COOCH2CH3+H2O.该反应类型是酯化(取代)反应. .
. +4NaOH$\stackrel{△}{→}$$→_{△}^{NaOH}$CH3COONa+
+4NaOH$\stackrel{△}{→}$$→_{△}^{NaOH}$CH3COONa+ +2H2O.
+2H2O.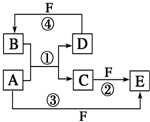 A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).