题目内容
设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A、常温常压下,11.2L氧气所含的原子数为NA |
| B、在常温常压下,22g二氧化碳中含有的原子数为1.5 NA |
| C、在标准状况下,5.6L四氯化碳含有的分子数为0.25NA |
| D、在非标准状况下,22.4LO2含有的分子数一定不是NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、气体摩尔体积vm=22.4L/mol使用条件是标准状况(0°C,101kPa);
B、二氧化碳分子中含有3个原子,22g二氧化碳的物质的量为0.5mol,含有1.5mol原子;
C、标况下,四氯化碳是液态;
D、非标准状况下,气体摩尔体积也可能是22.4L/mol.
B、二氧化碳分子中含有3个原子,22g二氧化碳的物质的量为0.5mol,含有1.5mol原子;
C、标况下,四氯化碳是液态;
D、非标准状况下,气体摩尔体积也可能是22.4L/mol.
解答:
解:A、不是标准状况,不能使用气体摩尔体积vm=22.4L/mol,11.2L氧气的物质的量不是0.5mol,所含的原子数不是NA,故A错误;
B.22g二氧化碳的物质的量为:
=0.5mol,0.5mol二氧化碳中含有1.5mol原子,含有的原子数为1.5NA,故B正确;
C、标况下,四氯化碳是液态,故C错误;
D、.由PV=nRT可知,在非标准状况下,气体摩尔体积也可能是22.4L/mol,故在非标准状况下,22.4L氧气的物质的量也可能是1mol,分子数也可能是NA个,故D错误;
故选B.
B.22g二氧化碳的物质的量为:
| 22g |
| 44g/mol |
C、标况下,四氯化碳是液态,故C错误;
D、.由PV=nRT可知,在非标准状况下,气体摩尔体积也可能是22.4L/mol,故在非标准状况下,22.4L氧气的物质的量也可能是1mol,分子数也可能是NA个,故D错误;
故选B.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在与Al反应能产生H2的溶液中,一定可以大量共存的离子组是( )
| A、NH4+、Al3+、Br-、SO42- |
| B、Na+、Mg2+、Cl-、NO3- |
| C、K+、Ba2+、ClO-、NO3- |
| D、K+、Na+、I-、SO42- |
已知标准状况下:①6.72L CH4②3.01×1023HCl ③23.1g CCl4④2.3g Na,下列对四种物质的关系由小到大表示正确的是( )
| A、体积 ④<①<②<③ |
| B、密度 ①<④<③<② |
| C、原子数 ④<③<②<① |
| D、质量 ④<①<③<② |
如图表示1~18号元素原子的结构或性质随核电荷数递增的变化.图中纵坐标表示( )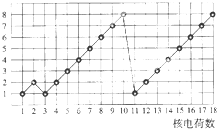

| A、最外层电子数 | B、原子半径 |
| C、最高化合价 | D、电子层数 |
已知Fe(OH)3胶粒带正电,向Fe(OH)3胶体中逐滴加入下列溶液,开始时出现红褐色沉淀,继续滴加沉淀逐渐溶解,则加入的溶液是( )
| A、2 mol?L-1NaOH溶液 |
| B、2 mol?L-1NaCl溶液 |
| C、2 mol?L-1NaHSO4溶液 |
| D、乙醇溶液 |
下列说法中正确的是( )
| A、1molO的质量是16g/mol |
| B、2g H2的物质的量是 1 |
| C、CO2的相对分子质量为44,1 molCO2的质量为44 g/mol |
| D、NaCl的摩尔质量是58.5g/mol |
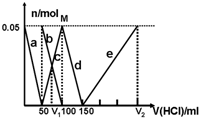 某Na2CO3、NaAlO2的混合溶液中逐滴加入1mol?L-1的盐酸,测得溶液中的CO32-、HCO3-、AlO2-、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示.则下列说法不正确的是( )
某Na2CO3、NaAlO2的混合溶液中逐滴加入1mol?L-1的盐酸,测得溶液中的CO32-、HCO3-、AlO2-、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示.则下列说法不正确的是( )| A、M点时生成的CO2为0 mol |
| B、V1:V2=1:4 |
| C、原混合溶液中的CO32-与AlO2-的物质的量之比为1:2 |
| D、a曲线表示的离子方程式为:AlO2-+H++H2O=Al(OH)3↓ |
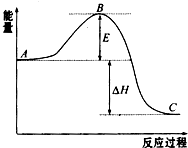 2SO2(g)+O2 (g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1
2SO2(g)+O2 (g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1