题目内容
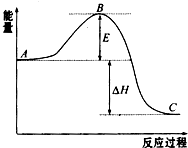 2SO2(g)+O2 (g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1
2SO2(g)+O2 (g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1请回答下列问题:
(1)图中A表示
(2)图中△H=
(3)如果反应速率v(SO2)为0.06mol?L-1?min-1,则v(O2)为
(4)已知S(s)+O2(g)=SO2(g)△H=-296kJ?mol-1,则由S(s)生成5mol SO3(g)的△H=
考点:反应热和焓变
专题:化学反应中的能量变化
分析:(1)A表示反应物总能量,B为活化能,活化能的大小与反应热无关;
(2)根据参加反应SO2的物质的量之比等于对应的△H之比;
(3)依据化学反应速率之比等于系数之比计算得到;
(4)根据已知的热化学方程式利用盖斯定律计算即可.
(2)根据参加反应SO2的物质的量之比等于对应的△H之比;
(3)依据化学反应速率之比等于系数之比计算得到;
(4)根据已知的热化学方程式利用盖斯定律计算即可.
解答:
解:(1)因图中A、C分别表示反应物总能量、生成物总能量,B为活化能,反应热可表示为A、C活化能的大小之差,活化能的大小与反应热无关,
故答案为:反应物能量;无;
(2)因1mol SO2(g)氧化为1mol SO3的△H=-99kJ?mol-1,所以2molSO2(g)氧化为2molSO3的△H=-198kJ?mol-1,
则2SO2(g)+O2(g)=2SO3(g)△H=-198KJ?mol-1,
故答案为:-198;
(3)反应的化学方程式为:2SO2(g)+O2(g)?2SO3(g),反应速率之比等于系数之比,v(SO2):v(O2):v(SO3)=2:1:2,反应速率υ(SO2)为0.06mol?L-1?min-1,依据比例计算得到v(O2)=0.03mol/L?min;
故答案为:0.03;
(4)已知①S(s)+O2(g)=SO2(g)△H1=-296 KJ?mol-1,②SO2(g)+
O2(g)=SO3(g)△H2=-99 KJ?mol-1;
则利用盖斯定律将①+②可得S(s)+
O2(g)=SO3(g)△H3=(△H1+△H2)=-395 KJ?mol-1,则由S(s)生成5mol SO3(g)的△H=-395×5 KJ?mol-1=-1975 KJ?mol-1;
故答案为:-1975 KJ?mol-1.
故答案为:反应物能量;无;
(2)因1mol SO2(g)氧化为1mol SO3的△H=-99kJ?mol-1,所以2molSO2(g)氧化为2molSO3的△H=-198kJ?mol-1,
则2SO2(g)+O2(g)=2SO3(g)△H=-198KJ?mol-1,
故答案为:-198;
(3)反应的化学方程式为:2SO2(g)+O2(g)?2SO3(g),反应速率之比等于系数之比,v(SO2):v(O2):v(SO3)=2:1:2,反应速率υ(SO2)为0.06mol?L-1?min-1,依据比例计算得到v(O2)=0.03mol/L?min;
故答案为:0.03;
(4)已知①S(s)+O2(g)=SO2(g)△H1=-296 KJ?mol-1,②SO2(g)+
| 1 |
| 2 |
则利用盖斯定律将①+②可得S(s)+
| 3 |
| 2 |
故答案为:-1975 KJ?mol-1.
点评:本题综合考查反应热与焓变,侧重于学生的分析能力和计算能力的考查,注意催化剂对反应的影响以及盖斯定律的应用,题目难度中等.

练习册系列答案
 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
室温下,甲、乙两烧杯均盛有5mLpH=3的某一元酸溶液,向乙烧杯中加水稀释至pH=4.关于甲、乙两烧杯中溶液的描述正确的是( )
| A、水电离出的OH-浓度:10c(OH-)甲≤c(OH-)乙 |
| B、溶液的体积:10V甲≤V乙 |
| C、若分别用等浓度的NaOH溶液完全中和,所得溶液的pH:甲≤乙 |
| D、若分别与5mLpH=11的NaOH溶液反应,所得溶液的pH:甲≥乙 |
常温下,将0.01mol/L的氢氧化钠溶液加水稀释10倍后,溶液的pH是( )
| A、2 | B、3 | C、0.001 | D、11 |
下列说法正确的是( )
| A、需要加热的化学反应都是吸热反应 |
| B、水力发电是将化学能转化为电能的过程 |
| C、某吸热反应能自发进行,因此该反应是熵增反应 |
| D、原电池是将电能转化为化学能的一种装置 |
根据下列化学方程式:2FeCl3+2KI=2FeCl2+2KCl+I2,2FeCl2+Cl2=2FeCl3,2KMnO4+16HCl=2MnCl2+5Cl2↑+8H2O+2KCl,判断各物质氧化性由强到弱的顺序正确是( )
| A、I2>Cl2>FeCl3>KMnO4 |
| B、KMnO4>Cl2>FeCl3>I2 |
| C、Cl2>I2>FeCl3>KMnO4 |
| D、FeCl3>KMnO4>Cl2>I2 |
将12mol/L的盐酸(ρ=1.19g/cm3)50mL稀释成6mol/L的盐酸(ρ=1.10g/cm3),需加水的体积为( )
| A、50mL |
| B、50.5mL |
| C、55mL |
| D、59.5mL |
设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A、常温常压下,11.2L氧气所含的原子数为NA |
| B、在常温常压下,22g二氧化碳中含有的原子数为1.5 NA |
| C、在标准状况下,5.6L四氯化碳含有的分子数为0.25NA |
| D、在非标准状况下,22.4LO2含有的分子数一定不是NA |
碘是人体中一种必需的微量元素.碘的元素符号是( )
| A、I | B、Cl | C、Br | D、Si |



