题目内容
 (1)CaC2中C22-与O22+互为等电子体,O22+的电子式可表示为
(1)CaC2中C22-与O22+互为等电子体,O22+的电子式可表示为(2)将乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2,红棕色沉淀.Cu+基态核外电子排布式为
(3)乙炔与氢氰酸反应可得丙烯腈(H2C=CH≡N).丙烯腈分子中碳原子轨道杂化类型是
(4)在合成氨反应中,催化剂铁表面上存在氮原子,如图为氮原子在铁的晶面上单层附着局部示意图(图中小黑色球代表氮原子,灰色球代表铁原子).则在如图示状况下,铁颗粒表面上
| N |
| Fe |
考点:共价键的形成及共价键的主要类型,配合物的成键情况,晶胞的计算,原子轨道杂化方式及杂化类型判断
专题:化学键与晶体结构
分析:(1)等电子体的结构相似,故O22+的电子式与C22-的电子式相似,含有2个π键和1个σ键;
(2)根据Cu为29号元素,根据电子排布式的书写方法来解答;根据[Cu(NH3)2]Cl分析;
(3)根据丙烯腈(H2C=CH-C≡N)中的C形成的δ键个数判断;
(4)根据氮原子在铁的晶面上的单层附着局部示意图可以看出,每个铁原子周围有2个氮原子,而每个氮原子周围有4个铁原子,据此答题.
(2)根据Cu为29号元素,根据电子排布式的书写方法来解答;根据[Cu(NH3)2]Cl分析;
(3)根据丙烯腈(H2C=CH-C≡N)中的C形成的δ键个数判断;
(4)根据氮原子在铁的晶面上的单层附着局部示意图可以看出,每个铁原子周围有2个氮原子,而每个氮原子周围有4个铁原子,据此答题.
解答:
解:(1)根据等电子体原理可知,O22+的电子式 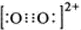 ,在1个O22+含有2个π键和1个σ键,则O22+中σ键数目和π键数目之为,1:2;
,在1个O22+含有2个π键和1个σ键,则O22+中σ键数目和π键数目之为,1:2;
故答案为: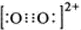 ;1:2;
;1:2;
(2)Cu为29号元素,要注意3d轨道写在4s轨道的前面,同时还有就是它的3d结构,Cu+的基态电子排布式为1s22s22p63s23p63d10,[Cu(NH3)2]Cl中为配体,则配位数为2;
故答案为:1s22s22p63s23p63d10;2;
(3)丙烯腈(H2C=CH-C≡N)中的C分别形成2个δ键和3个δ键,故碳原子的杂化轨道类型为sp和sp2杂化;
故答案为:sp、sp2;
(4)根据氮原子在铁的晶面上的单层附着局部示意图可以看出,每个铁原子周围有2个氮原子,而每个氮原子周围有4个铁原子,所以对于某个氮原子来讲,属于这个氮原子的铁原子数为4×
=2,所以氮原子与铁原子的个数比为1:2,
故答案为:1:2.
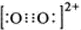 ,在1个O22+含有2个π键和1个σ键,则O22+中σ键数目和π键数目之为,1:2;
,在1个O22+含有2个π键和1个σ键,则O22+中σ键数目和π键数目之为,1:2;故答案为:
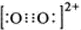 ;1:2;
;1:2;(2)Cu为29号元素,要注意3d轨道写在4s轨道的前面,同时还有就是它的3d结构,Cu+的基态电子排布式为1s22s22p63s23p63d10,[Cu(NH3)2]Cl中为配体,则配位数为2;
故答案为:1s22s22p63s23p63d10;2;
(3)丙烯腈(H2C=CH-C≡N)中的C分别形成2个δ键和3个δ键,故碳原子的杂化轨道类型为sp和sp2杂化;
故答案为:sp、sp2;
(4)根据氮原子在铁的晶面上的单层附着局部示意图可以看出,每个铁原子周围有2个氮原子,而每个氮原子周围有4个铁原子,所以对于某个氮原子来讲,属于这个氮原子的铁原子数为4×
| 1 |
| 2 |
故答案为:1:2.
点评:本题考查了学生对等电子体、Cu+基态核外电子排布、原子轨道杂化类型等知识,侧重于考查学生对基础知识的综合应用能力,难度中等,注意把握杂化轨道类型的判断方法.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
下列物质露置于干燥的空气中,不发生变化的是( )
| A、NaHCO3 |
| B、Na2O |
| C、Na2O2 |
| D、Na2CO3?10H2O |
在25℃和1.01×105Pa时,2N2O5(g)=4NO2(g)+O2(g);△H=+56.7kJ/mol,能自发进行的合理解释是( )
| A、是吸热反应 |
| B、是放热反应 |
| C、是熵减反应 |
| D、是熵增效应大于能量效应 |
实验测得 BeCl2为共价化合物,两个Be-Cl键间的夹角为180°则BeCl2属于( )
| A、由极性键构成的极性分子 |
| B、由极性键构成的非极性分子 |
| C、由非极性键构成的极性分子 |
| D、中心原子采用sp2杂化的分子 |
下列事实与胶体性质无关的是( )
| A、可用半透膜除去淀粉溶液中的少量NaCl |
| B、黄河入海口容易形成沙洲 |
| C、将植物油倒入水中用力搅拌可形成油水混合物 |
| D、一束平行光线通过蛋白质溶液,从侧面可以看到一条光亮的通路 |
下列说法中不正确的是( )
| A、标准状况下,等体积的CH4和CO2所含共用电子对数相等 |
| B、与NaOH溶液、H2SO4溶液反应产生等量H2,所需铝粉质量相等 |
| C、1 mol OH-和17 g NH3所含电子数相等 |
| D、明矾溶液中K+和Al3+物质的量浓度相等 |
下列指定反应的离子方程式正确的是( )
| A、Cu溶于稀硝酸HNO3:Cu+2H++NO3-=Cu2++NO2↑+H2O |
| B、试剂瓶玻璃塞被烧碱溶液腐蚀:SiO2+2Na++2OH-=Na2SiO3↓+H2O |
| C、向NaAlO2溶液中通入过量CO2:CO2+AlO2-+2H2O=Al(OH)3↓+HCO3- |
| D、用CH3COOH溶解CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑ |