题目内容
2.将15%的NaOH溶液蒸发掉100g水后得到质量分数为30%体积为95mL的NaOH溶液,则此时溶液的物质的量浓度为( )| A. | 7.9mol/L | B. | 6.25mol/L | C. | 6.75 mol/L | D. | 7 mol/L |
分析 蒸发前后溶质的质量不变,据此计算出蒸发前溶液的质量,根据质量分数计算溶质的物质的量,再由n=$\frac{m}{M}$、c=$\frac{n}{V}$计算蒸发后溶液的物质的量浓度.
解答 解:设15%的NaOH溶液的质量为x,蒸发前后溶质的质量不变,则有x×15%=(x-100g)×30%,解得x=200g,
故蒸发后溶液的质量为200g-100g=100g,
故30%的NaOH溶液中含有NaOH的物质的量为n=$\frac{100g×30%}{40g/mol}$=0.75mol,
所得溶液的物质的量浓度为$\frac{0.75mol}{0.095L}$=7.9mol/L
故选A.
点评 本题考查物质的量浓度的计算,为高频考点,把握蒸发前后溶质的质量不变为解答的关键,侧重分析与计算能力的考查,注意质量与物质的量的关系,题目难度不大.

练习册系列答案
相关题目
13. 把一块镁铝合金投入到1mol/LHCl溶液里,待合金完全溶解后,往溶液里加入1mol/LNaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积的变化关系如图所示.下列说法中不正确的是( )
把一块镁铝合金投入到1mol/LHCl溶液里,待合金完全溶解后,往溶液里加入1mol/LNaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积的变化关系如图所示.下列说法中不正确的是( )
 把一块镁铝合金投入到1mol/LHCl溶液里,待合金完全溶解后,往溶液里加入1mol/LNaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积的变化关系如图所示.下列说法中不正确的是( )
把一块镁铝合金投入到1mol/LHCl溶液里,待合金完全溶解后,往溶液里加入1mol/LNaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积的变化关系如图所示.下列说法中不正确的是( )| A. | a的取值范围为0≤a<50 | |
| B. | 当a=30时,$\frac{n(Mg)}{n(Al)}$=1 | |
| C. | 图中0~a段,与NaOH发生反应的微粒是H+ | |
| D. | 当v(NaOH)=90mL时,溶液中的溶质为NaAlO2 |
10.已知醋酸、醋酸根离子在溶液中存在下列平衡:
CH3COOH+H2O$\stackrel{高温}{?}$CH3COO-+H3O+ K1=1.75×10-5 mol•L-1,
CH3COO-+H2O$\stackrel{高温}{?}$CH3COOH+OH- K2=5.71×10-10mol•L-1
现将50mL 0.2mol•L-1醋酸与50mL 0.2mol•L-1醋酸钠溶液混合制得溶液甲,下列叙述正确的是( )
CH3COOH+H2O$\stackrel{高温}{?}$CH3COO-+H3O+ K1=1.75×10-5 mol•L-1,
CH3COO-+H2O$\stackrel{高温}{?}$CH3COOH+OH- K2=5.71×10-10mol•L-1
现将50mL 0.2mol•L-1醋酸与50mL 0.2mol•L-1醋酸钠溶液混合制得溶液甲,下列叙述正确的是( )
| A. | 溶液甲的pH>7 | |
| B. | 对溶液甲进行微热,K1、K2同时增大 | |
| C. | 溶液甲中,c(Na+)+c(H+)=c(CH3COO-) | |
| D. | 若在溶液甲中加入5 mL 0.1 mol•L-1的盐酸,则溶液中醋酸的K1会变大 |
17.下列实验中所选用的仪器合理的是( )
| A. | 用100mL量筒量取5.2mL的稀硫酸 | |
| B. | 用500mL容量瓶配制480mL 0.2mol/L的NaOH溶液 | |
| C. | 用托盘天平称量11.75克NaCl晶体 | |
| D. | 用分液漏斗进行固体和液体的分离 |
7.现有部分短周期主族元素的性质或原子结构如表:
(1)元素Z在周期表中的位置第3周期VⅡA族,XN2的结构式是:O=C=O,
(2)元素X的一种核素可测定文物年代,这种核素的符号是14C
(3)在X、Y最低价的简单氢化物中,较稳定的化合物的分子式是NH3.
(4)将少量W2N2固体投入到水中,剧烈反应,其反应的化学方程式为:2Na2O2+2H2O=4NaOH+O2↑.
(5)下列表述中,能证明元素Z与元素T非金属性的强弱的是B
A、常温下Z的单质和T的单质状态不同
B、Z的氢化物比T的氢化物稳定
C、一定条件下Z和T的单质都能与氢氧化钠溶液反应.
| 元素符号 | 原子结构和元素性质 |
| T | M层上有6个电子 |
| W | 短周期内原子半径最大 |
| N | 原子序数比T小,且与T同主族 |
| X | 最外层电子数是次外层的2倍 |
| Y | 常见单质为双原子分子且氢化物的水溶液呈碱性 |
| Z | 元素最高价为+7 |
(2)元素X的一种核素可测定文物年代,这种核素的符号是14C
(3)在X、Y最低价的简单氢化物中,较稳定的化合物的分子式是NH3.
(4)将少量W2N2固体投入到水中,剧烈反应,其反应的化学方程式为:2Na2O2+2H2O=4NaOH+O2↑.
(5)下列表述中,能证明元素Z与元素T非金属性的强弱的是B
A、常温下Z的单质和T的单质状态不同
B、Z的氢化物比T的氢化物稳定
C、一定条件下Z和T的单质都能与氢氧化钠溶液反应.
14.下列指定反应的离子方程式正确的是( )
| A. | 用盐酸除铁锈:Fe2O3•xH2O+6H+═2Fe3++(3+x)H2O | |
| B. | Mg(HCO3)2溶液与足量的 NaOH 溶液反应:Mg2++HCO3-+OH-═MgCO3↓+H2O | |
| C. | 强碱性溶液中次氯酸钠溶液与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3=2FeO42-+3Cl-+H2O+4H+ | |
| D. | 用NaOH 溶液吸收 NO2:2NO2+2OH-═2NO3-+H2O |
12.下列实验能达到实验目的是( )
| A. |  制取金属锰 | |
| B. |  制取二氧化碳 | |
| C. |  蒸发饱和食盐水制取食盐晶体 | |
| D. |  验证FeCl3对H2O2分解反应有催化作用 |
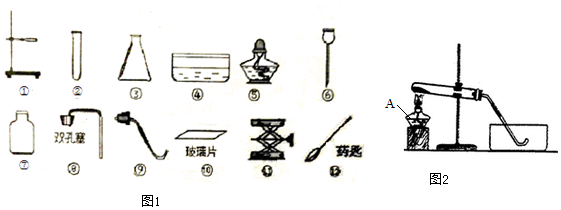
 ;
; ;
; ,写出C2B2与A2B反应的离子方程式2Na2O2+2H2O═4Na++4OH-+O2↑;
,写出C2B2与A2B反应的离子方程式2Na2O2+2H2O═4Na++4OH-+O2↑;