题目内容
把物质的量均为0.1mol的AlCl3、CuCl2和H2SO4溶于水制成100mL的混合溶液,用石墨做电极电解,并收集两电极所产生的气体,一段时间后在两极收集到的气体在相同条件下体积相同.则
(1)两个电极均可收集到的气体在标准状况下的体积为 L;
(2)电路中共转移 mol电子;
(3)铝元素最终的存在形式为 .
(1)两个电极均可收集到的气体在标准状况下的体积为
(2)电路中共转移
(3)铝元素最终的存在形式为
考点:电解原理
专题:电化学专题
分析:AlCl3、CuCl2和H2SO4溶于水制成的混合溶液,用石墨做电极电解,则阴极上发生的电极反应为:Cu2++2e-=Cu,2H++2e-=H2↑,阳极上发生电极反应:Cl--2e-=Cl2↑,4OH-→O2↑+2H2O+4e-,根据电子守恒和电极方程式进行计算即可.
解答:
解:(1)阴极上发生的电极反应为:Cu2++2e-=Cu,2H++2e-=H2↑,阳极上发生电极反应:Cl--2e-=Cl2↑,4OH-→O2↑+2H2O+4e-,可知Cu2+全部反应,Cu2+0.1mol,Cl-反应完全,在阴极上:Cu2++2e-=Cu,铜离子全部放电转移电子是0.2mol,2H++2e-=H2↑,(Cu2+全部反应,H+开始电解,这段相当于电解HCl)
在阳极上:Cl--e-=
Cl2↑,氯离子全部放电转移电子是0.5mol,产生氯气是0.25mol;4OH--4e-=2H2O+O2,设两极上转移电子是x,则0.25+
×(x-0.5)=
(x-0.2),解得x=0.9mol,两个电极均可收集到的气体在标准状况下的体积为0.5(0.9-0.2)mol×22.4L/mol=7.84L,
故答案为:7.84;
(2)由(1)分析可知电路中转移的电子是0.9mol,故答案为:0.9;
(3)Al3+移向阴极,该电极上的电极反应:阴极上发生的电极反应为:Cu2++2e-=Cu,2H++2e-=H2↑,铜离子全部放电转移电子是0.2mol,转移电子0.9mol,则消耗氢离子0.7mol,原溶液中含有0.2molH+,消耗的OH-0.4mol,相当于多出来0.1molOH-,Al3+0.1mol,OH-0.1mol,所以溶液中以Al3+形式存在,还有Al(OH)3沉淀,即铝元素仅以铝离子和Al(OH)3的形式存在,
故答案为:Al3+ 和Al(OH)3.
在阳极上:Cl--e-=
| 1 |
| 2 |
| 1 |
| 4 |
| 1 |
| 2 |
故答案为:7.84;
(2)由(1)分析可知电路中转移的电子是0.9mol,故答案为:0.9;
(3)Al3+移向阴极,该电极上的电极反应:阴极上发生的电极反应为:Cu2++2e-=Cu,2H++2e-=H2↑,铜离子全部放电转移电子是0.2mol,转移电子0.9mol,则消耗氢离子0.7mol,原溶液中含有0.2molH+,消耗的OH-0.4mol,相当于多出来0.1molOH-,Al3+0.1mol,OH-0.1mol,所以溶液中以Al3+形式存在,还有Al(OH)3沉淀,即铝元素仅以铝离子和Al(OH)3的形式存在,
故答案为:Al3+ 和Al(OH)3.
点评:本题考查学生电解池的工作原理知识,可以根据所学内容来回答,难度较大.

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案
相关题目
下列溶液中,跟100mL 0.5mol/L NaCl溶液所含的Cl-物质的量浓度相同的是( )
| A、100mL 0.5mol/L MgCl2溶液 |
| B、200mL 0.25mol/L AlCl3溶液 |
| C、50mL 1mol/L NaCl溶液 |
| D、25mL 0.5mol/L HCl溶液 |
下列属于物理变化的是( )
| A、煤的干馏 | B、石油的裂解 |
| C、煤的气化 | D、石油的分馏 |
取质量均为m g的铁铜混合物四份,分别加入同浓度,不同体积的稀硝酸充分反应,在标准状况下生成NO(设还原产物只有一种)体积与剩余固体金属的质量如表.下列判断不正确的是( )
| 实验编号 | 1 | 2 | 3 | 4 |
| 稀HNO3体积(mL) | 100 | 200 | 300 | 400 |
| 剩余金属质量(g) | 9.0 | 4.8 | 0 | 0 |
| NO体积(L) | 1.12 | 2.24 | 3.36 | V |
| A、实验1中溶解的金属是铁且质量为4.2g |
| B、实验2中4.8g金属的组成是铁与铜 |
| C、实验4发生反应的离子方程式:3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O |
| D、实验4中V的数值为4.48 |
由锌、铁、铝、镁四种金属中的两种组成的合金10g,与足量的盐酸反应产生的氢气在标准状况下为11.2L,则此合金可能是( )
| A、锌 镁 |
| B、铁 铝 |
| C、铁 锌 |
| D、镁 铁 |
下列各组物质总物质的量一定,两种物质以任何比例相混合并充分燃烧,生成H2O和CO2的物质的量之比始终不变的是( )
①甲醇和乙醛 ②乙烷和乙烯 ③乙炔和苯 ④乙酸和葡萄糖
⑤乙醇和甲醚 ⑥丙醛和甲醚 ⑦苯酚和苯二酚.
①甲醇和乙醛 ②乙烷和乙烯 ③乙炔和苯 ④乙酸和葡萄糖
⑤乙醇和甲醚 ⑥丙醛和甲醚 ⑦苯酚和苯二酚.
| A、③④⑤⑦ | B、③④⑥⑦ |
| C、①②⑤⑥ | D、①③⑤⑥ |
CO和CO2混合气体含碳元素36%,取此混合气体10g,通过足量灼热的CuO后,将气体通过足量的澄清石灰水,得到白色沉淀的质量是( )
| A、5g | B、10g |
| C、20g | D、30g |
下列气体均被计入空气污染指数的一组是( )
| A、二氧化硫、二氧化氮、氮气 |
| B、二氧化硫、二氧化氮、一氧化碳 |
| C、二氧化硫、一氧化碳、二氧化碳 |
| D、二氧化氮、一氧化碳、水蒸气 |
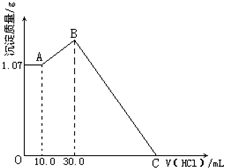 将FeCl3、AlCl3两种固体混合物溶于足量水后加入一定量的NaOH溶液,产生1.07g红褐色沉淀,再向所得浊液中逐滴滴加1.00mol?L-1HCl溶液,加入HCl溶液的体积与生产沉淀的关系如图所示,试回答:
将FeCl3、AlCl3两种固体混合物溶于足量水后加入一定量的NaOH溶液,产生1.07g红褐色沉淀,再向所得浊液中逐滴滴加1.00mol?L-1HCl溶液,加入HCl溶液的体积与生产沉淀的关系如图所示,试回答: