题目内容
15.下列电极反应式与出现的环境相匹配的是( )| 选项 | 电极反应式 | 出现的环境 |
| A | O2+2H2O+4e-═4OH- | 碱性环境下氢氧燃料电池的负极反应 |
| B | 4OH--4e-═O2↑+2H2O | 弱酸性环境下钢铁的吸氧腐蚀 |
| C | Cu-2e-═Cu2+ | 用铜做电极电解NaOH溶液的阳极反应 |
| D | H2-2e-═2H+ | 用惰性电极电解H2SO4溶液的阳极反应 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.碱性条件下的氢氧燃料电池中,氢气在负极上失电子发生氧化反应,氧气在正极上得电子发生还原反应;
B.弱酸性环境下,钢铁发生吸氧腐蚀,正极上氧气得电子发生还原反应;
C.用铜作电极电解氢氧化钠溶液,阳极铜是活性电极,优先溶液中的阴离子失电子发生氧化反应,阴极上阳离子氢离子优先得电子发生还原反应;
D.用惰性电极电解H2SO4溶液时,阳极上氢氧根离子优先失电子发生氧化反应.
解答 解:A.碱性条件下的氢氧燃料电池中,氢气在负极上的电极反应式为:H2-2e-+2OH-=2H2O,故A错误;
B.弱酸性环境下钢铁的吸氧腐蚀,正极上氧气得电子生成氢氧根离子,电极反应式为:O2↑+2H2O+4e-=4OH-,故B错误;
C.用铜做电极电解NaOH溶液时,阳极铜是活性电极,放电能力强于溶液中的氢氧根,电极反应式为:Cu-2e-═Cu2+,故C正确;
D.用惰性电极电解H2SO4溶液时,阳极上氢氧根离子放电能力强于硫酸根离子,电极反应式为:4OH--4e-=O2↑+2H2O,故D错误;
故选C.
点评 本题考查原电池和电解池原理,明确阴阳极和正负极上的反应类型是解本题的关键,注意电解池中离子的放电顺序,铜作电解池阳极时,阳极上铜失电子而不是溶液中阴离子失电子,为易错点.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
20.目前,我市电能的主要来源是火力发电. 下列关于火力发电过程中能量转化关系的描述,正确的是( )

| A. | 化学能转化成机械能在转化成电能 | |
| B. | 化学能转化成热能在转化成电能 | |
| C. | 化学能转化成机械能在转化成热能在到机械能 | |
| D. | 化学能转化成热能在转化成机械能在到电能 |
3.硫化钠(Na2S)在工业上用途广泛.某课题组用无水Na2SO4制备硫化钠的流程如下:
①取一定量的无水Na2SO4和碳粉进行隔绝空气高温灼烧;
②将灼烧产物冷却后,加入NaOH溶液进行碱浸
③过滤,滤液经过一系列的操作步骤后得到硫化钠晶体.
(1)过滤需要用到的主要玻璃仪器是漏斗、烧杯、玻璃棒.
(2)若灼烧所得气体为等物质的量的CO和CO2,写出灼烧时发生的化学反应方程为3Na2SO4+8C$\frac{\underline{\;\;△\;\;}}{\;}$3Na2S+4CO2↑+4CO↑.
(3)上述流程中采用a浸洗更好.
a.稀NaOH溶液b.热水c.氨水d.乙醇
(4)固体产物Na2S晶体中可能含有杂质,该课题组对固体产物的杂质成分提出以下假设:
假设一:杂质成分为NaOH;
假设二:杂质成分为Na2SO4;
假设三:杂质成分为NaOH和Na2SO4.
为验证假设三成立,课题组进行如下研究,请你完成下表中的内容:
:
①取一定量的无水Na2SO4和碳粉进行隔绝空气高温灼烧;
②将灼烧产物冷却后,加入NaOH溶液进行碱浸
③过滤,滤液经过一系列的操作步骤后得到硫化钠晶体.
(1)过滤需要用到的主要玻璃仪器是漏斗、烧杯、玻璃棒.
(2)若灼烧所得气体为等物质的量的CO和CO2,写出灼烧时发生的化学反应方程为3Na2SO4+8C$\frac{\underline{\;\;△\;\;}}{\;}$3Na2S+4CO2↑+4CO↑.
(3)上述流程中采用a浸洗更好.
a.稀NaOH溶液b.热水c.氨水d.乙醇
(4)固体产物Na2S晶体中可能含有杂质,该课题组对固体产物的杂质成分提出以下假设:
假设一:杂质成分为NaOH;
假设二:杂质成分为Na2SO4;
假设三:杂质成分为NaOH和Na2SO4.
为验证假设三成立,课题组进行如下研究,请你完成下表中的内容:
| 实验步骤 | 预期的实验现象和结论 |
| 步骤:取一定量的固体产物于试管中,加入适量蒸馏水进行溶解,然后往试管中加入适量的 CuCl2溶液并过滤. | \ |
| 步骤2: 取1的滤液加入酚酞试液,若溶液变红, | 说明有NaOH |
| 步骤3: 取1的滤液加入BaCl2溶液,若产生白色沉淀, | 说明有Na2SO4 |
10.“绿色化学”的主要内容之一是从技术、经济上设计可行的化学反应,使原子充分利用,不产生污染物.下列化学反应不符合“绿色化学”理念的是( )
| A. | 制氯乙烷:CH2=CH2+HCl$→_{△}^{催化剂}$CH3CH2Cl | |
| B. | 制甲基丙烯酸甲酯:CH3C≡CH+CO+CH3OH $\stackrel{Pd}{→}$ CH2=C(CH3)COOCH3 | |
| C. | 制CuSO4:2Cu+O2=2CuO,CuO+H2SO4(稀)═CuSO4+H2O | |
| D. | 制Cu(NO3)2:Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O |
20.某工业废水中仅含表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为0.1mol/L.
甲同学欲探究废水的组成,进行了如下实验:
I.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察).
Ⅱ.取少量溶液,加入KSCN溶液无明显变化.
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变.
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成.
请推断:
(1)由I、Ⅱ判断,溶液中一定不含有的阳离子是K+、Fe3+(写离子符号).
(2)Ⅲ中加入少量盐酸生成无色气体的离子方程式是3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O.
(3)将Ⅲ中红棕色气体(标况下)收集一满试管然后倒扣入水中(假设溶质不扩散),所得溶液的物质的量浓度为0.045mol/L(精确到千分位).
(4)甲同学最终确定原溶液中所含阳离子是Fe2+、Cu2+,阴离子是Cl-、NO3-、SO42-.(写离子符号)
(5)另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体为CuO和Fe2O3质量为1.6g.
| 阳离子 | K+ Cu2+ Fe3+ Al3+ Fe2+ |
| 阴离子 | Cl- CO32- NO3- SO42- SiO32- |
I.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察).
Ⅱ.取少量溶液,加入KSCN溶液无明显变化.
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变.
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成.
请推断:
(1)由I、Ⅱ判断,溶液中一定不含有的阳离子是K+、Fe3+(写离子符号).
(2)Ⅲ中加入少量盐酸生成无色气体的离子方程式是3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O.
(3)将Ⅲ中红棕色气体(标况下)收集一满试管然后倒扣入水中(假设溶质不扩散),所得溶液的物质的量浓度为0.045mol/L(精确到千分位).
(4)甲同学最终确定原溶液中所含阳离子是Fe2+、Cu2+,阴离子是Cl-、NO3-、SO42-.(写离子符号)
(5)另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体为CuO和Fe2O3质量为1.6g.
4.用镍黑合金提取高纯氢的方法属于( )
| A. | 重结晶纯化法 | B. | 萃取纯化法 | C. | 吸附纯化法 | D. | 蒸馏纯化法 |
5.下列化学用语正确的是( )
| A. | 氮分子的结构式 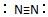 | B. | 硫原子的结构示意图 | ||
| C. | 氯化钠的电子式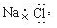 | D. | 水分子的结构式 H-O-H |
 .
.