题目内容
(1)分别完全燃烧①1molCH4、②1molC2H4、③1molC6H6,生成的水相等的是 ;(填序号,下同)需要的氧气最多的是 .
(2)0.1mol某烃完全燃烧,生成10.8g H2O和11.2LCO2(标准状况下).则该烃的分子式: ;在其同分异构体中,一氯代物只有一种的结构简式是: .
(2)0.1mol某烃完全燃烧,生成10.8g H2O和11.2LCO2(标准状况下).则该烃的分子式:
考点:化学方程式的有关计算,有关有机物分子式确定的计算
专题:
分析:(1)各烃的物质的量相等,生成水相等,则烃分子中H原子数目相等;根据1mol烃CxHy耗氧量(x+
)mol判断;
(2)计算水、二氧化碳的物质的量,根据原子守恒确定烃的分子式;其一氯代物只有原子,则分子中只含有1种H原子,进而书写一氯代物只有一种的结构简式.
| y |
| 4 |
(2)计算水、二氧化碳的物质的量,根据原子守恒确定烃的分子式;其一氯代物只有原子,则分子中只含有1种H原子,进而书写一氯代物只有一种的结构简式.
解答:
解:(1)各烃的物质的量相等,生成水相等,根据H原子守恒,则烃分子中H原子数目相等,故生成的水相等的是①CH4与②C2H4;
①1molCH4耗氧量为(1+1)mol=2mol,②1molC2H4的耗氧量为(2+1)mol=3mol,③1molC6H6的耗氧量为(6+
)mol=7.5mol,故C6H6的耗氧量最多,
故答案为:①②;③;
(2)10.8g H2O的物质的量为
=0.6mol,11.2LCO2(标准状况下)的物质的量为
=0.5mol,则有机物分子中N(C)=
=5、N(H)=
=12,故该烃的分子式为C5H12,其同分异构体中,一氯代物只有一种的结构简式是: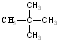 ,
,
故答案为:C5H12; .
.
①1molCH4耗氧量为(1+1)mol=2mol,②1molC2H4的耗氧量为(2+1)mol=3mol,③1molC6H6的耗氧量为(6+
| 6 |
| 4 |
故答案为:①②;③;
(2)10.8g H2O的物质的量为
| 10.8g |
| 18g/mol |
| 11.2L |
| 22.4L/mol |
| 0.5mol |
| 0.1mol |
| 0.6mol×2 |
| 0.1mol |
 ,
,故答案为:C5H12;
 .
.
点评:本题考查烃燃烧有关计算、有机物分子式确定、同分异构体书写,难度不大,注意掌握有机物燃烧有关规律.

练习册系列答案
相关题目
3.0g某有机样品完全燃烧,燃烧后的混合物通入过量的澄清石灰水中,石灰水共增重6.2g,经过滤得到10g沉淀.该有机样品的组成可能是( )
| A、葡萄糖与蔗糖 |
| B、醋酸与果糖 |
| C、乙醇与葡萄糖 |
| D、乙醛与葡萄糖 |
某有机物A由C、H、O三种元素组成,相对分子质量为90.将9.0g A 完全燃烧的产物依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g.A能与NaHCO3溶液反应,且2分子A之间脱水可生成六元环化合物.有关A的说法正确的是( )
| A、0.1 mol A与足量Na反应产生2.24 L H2(标准状况) |
| B、分子式是C3H8O3 |
| C、A催化氧化的产物能发生银镜反应 |
D、A在一定条件下发生缩聚反应的产物是: |
燃料电池是一种高效、环境友好的发电装置,它的原理是原电池原理,可进行能量的转换.以CH4为燃料时,另一极通入氧气,以KOH为电解质溶液,产物为碳酸钾和水,二氧化碳的排放量比常规发电减少40%以上.下列有关燃料电池的说法正确的是( )
| A、通入甲烷的一极是燃料电池的负极,该电极上发生的是还原反应 |
| B、燃料电池是将热能转换为电能的装置 |
| C、通入氧气的一极的电极反应是:O2+4e-+2H2O=4OH- |
| D、该燃料电池使用一段时间后,溶液的c(OH-)增大 |
在实验时,为防止下列情况发生,采取的措施错误的是( )
| A、制取蒸馏水时,为防止烧瓶内产生暴沸现象,应先向烧瓶中加入几片碎瓷片 |
| B、在用系列实验装置制取Cl2和检验Cl2的实验中,尾气污染空气,应用水吸收尾气 |
| C、用加热KMnO4的方法制得的氧气中带有紫色,应在靠近试管口的地方放一团棉花 |
| D、由石灰石制CO2气体时,应用NaOH溶液吸收其尾气 |
 在体积为V L的恒容密闭容器中盛有一定量H2,通入Br2(g)发生反应:H2(g)+Br2(g)?2HBr(g)△H<0.当温度分别为T1、T2,平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示.下列说法不正确的是( )
在体积为V L的恒容密闭容器中盛有一定量H2,通入Br2(g)发生反应:H2(g)+Br2(g)?2HBr(g)△H<0.当温度分别为T1、T2,平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示.下列说法不正确的是( )| A、由图可知:T1>T2 |
| B、a、b两点的反应速率:a<b |
| C、为了提高Br2(g)的转化率,可采取将HBr液化并及时移走的方法 |
| D、T1时,随着Br2(g)加入,平衡时HBr的体积分数不断增加 |
 如图中的四条线表示钠、镁、铝、铁分别和足量Cl2反应时,消耗金属的质量(纵轴)与参加反应的氯气质量(横轴)的关系,其中代表铁与氯气反应的是( )
如图中的四条线表示钠、镁、铝、铁分别和足量Cl2反应时,消耗金属的质量(纵轴)与参加反应的氯气质量(横轴)的关系,其中代表铁与氯气反应的是( )