题目内容
3.0g某有机样品完全燃烧,燃烧后的混合物通入过量的澄清石灰水中,石灰水共增重6.2g,经过滤得到10g沉淀.该有机样品的组成可能是( )
| A、葡萄糖与蔗糖 |
| B、醋酸与果糖 |
| C、乙醇与葡萄糖 |
| D、乙醛与葡萄糖 |
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:根据题意,3.0 g有机样品燃烧生成CO2和H2O的总质量为6.2 g.10 g碳酸钙的物质的量为0.1 mol,含0.1 mol C,则CO2的物质的量为0.1 mol,故生成水的质量为6.2 g-0.1 mol×44 g?mol-1=1.8 g,其物质的量为0.1 mol,含0.2 mol H.因此,3.0 g样品中氧原子的质量为3.0 g-0.1 mol×12 g?mol-1-0.2 mol×1 g?mol-1=1.6 g,其物质的量为0.1 mol.各元素原子个数之比为:N(C):N(H):N(O)=0.1:0.2:0.1=1:2:1,实验式为CH2O,混合物如满足最简式符合CH2O即可,以此解答该题.
解答:
解:根据题意,3.0 g有机样品燃烧生成CO2和H2O的总质量为6.2 g.10 g碳酸钙的物质的量为
=0.1 mol,
含0.1 mol C,则CO2的物质的量为0.1 mol,故生成水的质量为6.2 g-0.1 mol×44 g?mol-1=1.8 g,
其物质的量为
=0.1 mol,含0.2 mol H.
因此,3.0 g样品中氧原子的质量为3.0 g-0.1 mol×12 g?mol-1-0.2 mol×1 g?mol-1=1.6 g,
其物质的量为
=0.1 mol.
各元素原子个数之比为:N(C):N(H):N(O)=0.1:0.2:0.1=1:2:1,实验式为CH2O,
A.葡萄糖与蔗糖的分子式分别为C6H12O6、C12H22O11,实验式不都为CH2O,故A错误;
B.醋酸与果糖的分子式分别为C2H4O2、C6H12O6,实验式为CH2O,故B正确;
C.乙醇与葡萄糖的分子式分别为C2H6O2、C6H12O6,实验式不都为CH2O,故C错误;
D.乙醛与葡萄糖的分子式分别为C2H4O、C6H12O6,实验式不都为CH2O,故D错误.
故选B.
| 10g |
| 100g/mol |
含0.1 mol C,则CO2的物质的量为0.1 mol,故生成水的质量为6.2 g-0.1 mol×44 g?mol-1=1.8 g,
其物质的量为
| 1.8g |
| 18g/mol |
因此,3.0 g样品中氧原子的质量为3.0 g-0.1 mol×12 g?mol-1-0.2 mol×1 g?mol-1=1.6 g,
其物质的量为
| 1.6g |
| 16g/mol |
各元素原子个数之比为:N(C):N(H):N(O)=0.1:0.2:0.1=1:2:1,实验式为CH2O,
A.葡萄糖与蔗糖的分子式分别为C6H12O6、C12H22O11,实验式不都为CH2O,故A错误;
B.醋酸与果糖的分子式分别为C2H4O2、C6H12O6,实验式为CH2O,故B正确;
C.乙醇与葡萄糖的分子式分别为C2H6O2、C6H12O6,实验式不都为CH2O,故C错误;
D.乙醛与葡萄糖的分子式分别为C2H4O、C6H12O6,实验式不都为CH2O,故D错误.
故选B.
点评:本题考查有机物分子式的确定,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握有机物实验式的确定,难度中等.

练习册系列答案
相关题目
甲、乙两容器中均进行反应:N2+3H2?2NH3,在相同时间内,甲容器中断裂1molN≡N键且同时形成3molH-H键,乙容器中断裂0.5molN≡N键且同时断裂3molN-H键,下列说法正确的是( )
| A、甲容器中的反应速率一定大于乙容器中的反应速率 |
| B、甲容器中的反应速率可能小于乙容器中的反应速率 |
| C、无法判断两容器中的上述反应是否都达到了平衡状态 |
| D、上述两容器中的反应一定是在相同温度和相同压强下进行的 |
1mol某烃在氧气中充分燃烧,需要消耗氧气179.2L(标准状况下).它在光照的条件下与氯气反应能生成三种不同的一氯取代物.该烃的结构简式是( )
A、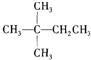 |
| B、CH3CH2CH2CH2CH3 |
C、 |
D、 |
下列物质的浓溶液,能用磨口玻璃试剂瓶盛放的是( )
| A、浓H2SO4 |
| B、水玻璃 |
| C、苛性钾 |
| D、氢氟酸 |
 二氧化氯(ClO2)是~种高效消毒剂,沸点为11℃.用氯酸钾粉末与草酸在60℃时反应可生成二氧化氯等物质,实验装置如下图所示:
二氧化氯(ClO2)是~种高效消毒剂,沸点为11℃.用氯酸钾粉末与草酸在60℃时反应可生成二氧化氯等物质,实验装置如下图所示: 写出反应方程式
写出反应方程式 如图表示一个晶胞,该晶胞为正方体型,原子(或分子、离子)位于正方体的顶点和面心.试回答下列问题:
如图表示一个晶胞,该晶胞为正方体型,原子(或分子、离子)位于正方体的顶点和面心.试回答下列问题: