题目内容
(1)用电子式表示Na2O的形成过程: ;用电子式表示H2O的形成过程:
(2)写出下列物质的电子式
N2 H2O2 NH3 NaOH MgBr2 .
(2)写出下列物质的电子式
N2
考点:用电子式表示简单的离子化合物和共价化合物的形成,电子式
专题:
分析:(1)氧化钠为离子化合物、水为共价化合物,根据离子化合物和共价化合物的电子式的表示方法写出用电子式表示二者的形成过程;
(2)氮气分子中存在氮氮三键,氮原子最外层为8电子;
双氧水为共价化合物,其分子中存在两个氧氢键和1个氧氧键;
NH3属于共价化合物,不存在离子键,分子中存在3对共用电子对,氮原子最外层为8个电子;
氢氧化钠为离子化合物,电子式中需要标出阴阳离子所带电荷,氢氧根离子需要标出最外层电子;
溴化镁为离子化合物,镁离子直接用离子符号表示,溴离子需要标出最外层电子及所带电荷.
(2)氮气分子中存在氮氮三键,氮原子最外层为8电子;
双氧水为共价化合物,其分子中存在两个氧氢键和1个氧氧键;
NH3属于共价化合物,不存在离子键,分子中存在3对共用电子对,氮原子最外层为8个电子;
氢氧化钠为离子化合物,电子式中需要标出阴阳离子所带电荷,氢氧根离子需要标出最外层电子;
溴化镁为离子化合物,镁离子直接用离子符号表示,溴离子需要标出最外层电子及所带电荷.
解答:
解:(1)Na2O为离子化合物,用电子式表示Na2O的形成过程为: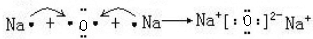 ;
;
H2O为共价化合物,各原子达到稳定结构,用电子式表示形成过程: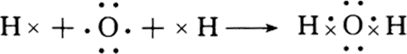 ,
,
故答案为: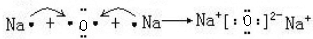 ;
;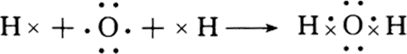 ;
;
(2)N2分子中存在氮氮三键,氮气的电子式为: ;
;
(3)NH3为共价化合物,氨气分子中存在3个氮氢键,则氨气的电子式为: ;
;
H2O2为共价化合物,其电子式为: ;
;
NaOH为离子化合物,氢氧化钠的电子式为: ;
;
Mg失去2个电子,被2个溴原子分别得到1个形成溴离子,则溴化镁的电子式为: .
.
故答案为: ;
; ;
; ;
; ;
; ,
,
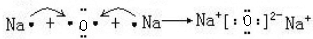 ;
;H2O为共价化合物,各原子达到稳定结构,用电子式表示形成过程:
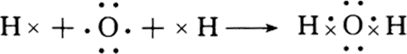 ,
,故答案为:
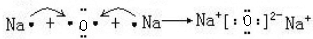 ;
;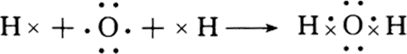 ;
;(2)N2分子中存在氮氮三键,氮气的电子式为:
 ;
;(3)NH3为共价化合物,氨气分子中存在3个氮氢键,则氨气的电子式为:
 ;
;H2O2为共价化合物,其电子式为:
 ;
;NaOH为离子化合物,氢氧化钠的电子式为:
 ;
;Mg失去2个电子,被2个溴原子分别得到1个形成溴离子,则溴化镁的电子式为:
 .
.故答案为:
 ;
; ;
; ;
; ;
; ,
,
点评:本题考查了电子式的书写,题目难度中等,试题题量较大,充分考查了学生对书写知识的掌握情况,注意掌握离子化合物与共价化合物电子式的书写原则,试题有利于培养学生灵活应用所学知识的能力.

练习册系列答案
相关题目
下列物质的浓溶液,能用磨口玻璃试剂瓶盛放的是( )
| A、浓H2SO4 |
| B、水玻璃 |
| C、苛性钾 |
| D、氢氟酸 |
1866年凯库勒提出了苯的单、双键交替的正六边形平面结构,解释了苯的部分性质,但还有一些问题尚未解决,它不能解释下列事实( )
| A、苯不能使溴水褪色 |
| B、苯能与H2发生加成反应 |
| C、溴苯没有同分异构体 |
| D、苯能燃烧 |
 如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈蓝色.下列说法中不正确的是( )
如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈蓝色.下列说法中不正确的是( )| A、x是正极,y是负极 |
| B、x是负极,y是正极 |
| C、a极和Pt都有气泡产生 |
| D、U形管中溶液的碱性增强 |
下列能源组合中,均属于新能源的一组是( )
①天然气;②煤;③核能;④石油;⑤太阳能;⑥生物质能;⑦风能;⑧氢能.
①天然气;②煤;③核能;④石油;⑤太阳能;⑥生物质能;⑦风能;⑧氢能.
| A、①②③④ |
| B、①⑤⑥⑦⑧ |
| C、③④⑤⑥⑦⑧ |
| D、③⑤⑥⑦⑧ |
盐酸、醋酸、碳酸钠和碳酸氢钠是生活中常见的物质,下列表述正确的是( )
| A、在Na2CO3溶液中加入与其溶质等物质的量的冰醋酸,溶液中存在:c(Na+)=c(CH3COOH)+c(CH3COO-)+c(CO32-)+c(HCO3-)+c(H2CO3) |
| B、NaHCO3溶液中存在:c(H+)+c(H2CO3)=c(OH-) |
| C、10 mL 1.0 mol?L-1CH3COOH溶液中加入0.01 mol的NaOH后,溶液中离子浓度的大小关系为:c(Na+)=c(CH3COO-)>c(OH-)=c(H+) |
| D、相同条件下,中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗的NaOH物质的量前者大 |

