题目内容
在温度和压强不变的情况下,反应2NO2?2NO+O2达到平衡,若反应前NO2为0.5L,反应后混合气体的体积变为0.65L,则NO2的分解率是( )
| A、15% | B、20% |
| C、60% | D、75% |
考点:化学平衡的计算
专题:化学平衡专题
分析:根据体积变化,利用方程式差量法计算参加反应的NO2的体积,再根据NO2的转化率=
×100%计算.
| 消耗量 |
| 起始量 |
解答:
解:令参加反应的NO2的体积为V,则:
2NO2?2NO+O2 体积增大△V
2 (2+1)-2=1
V 0.65L-0.5L=0.15L
所以 2:1=V:0.15L
解得:V=0.3L
所以NO2的转化率=
×100%=60%,
故选C.
2NO2?2NO+O2 体积增大△V
2 (2+1)-2=1
V 0.65L-0.5L=0.15L
所以 2:1=V:0.15L
解得:V=0.3L
所以NO2的转化率=
| 0.3L |
| 0.5L |
故选C.
点评:本题考查化学平衡的有关计算,难度中等,注意差量法的理解与利用.

练习册系列答案
相关题目
下列说法正确的是( )
| A、纤维素属于髙分子化合物,与淀粉互为同分异构体,水解后均生成葡萄糖 |
| B、2,3一二甲基丁烷的H一NMR上有5个峰 |
| C、含5个碳原子的有机物,每个分子中最多可形成4个C一C单键 |
D、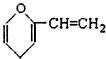 某有机物结构如图所示,该有机物属于芳香族化合物的同分异构体有5种,其中遇FeCl3能显色的有3种 |
将24ml的NO2、NO混合气体和12ml的O2通入倒立在水槽中盛有水的量筒内,充分反应后,量筒里液面上升,最终剩余3ml气体,则原混合气体中NO的体积为( )
①16ml ②16.5ml ③7.5ml ④6ml ⑤18ml ⑥12ml.
①16ml ②16.5ml ③7.5ml ④6ml ⑤18ml ⑥12ml.
| A、①② | B、⑤⑥ | C、③④ | D、②④ |
在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:SnCl2+Cl-+H3AsO3+H+-As+SnCl
+M(未配平),关于该反应的说法中正确的组合是( )
①氧化剂是H3AsO3
②还原性:Cl->As
③每生成0.1mol的As,还原剂失去的电子为0.3mol
④M为OH-
⑤SnCl
是氧化产物
⑥H+前面的配平系数为6.
2- 0 |
①氧化剂是H3AsO3
②还原性:Cl->As
③每生成0.1mol的As,还原剂失去的电子为0.3mol
④M为OH-
⑤SnCl
2- 0 |
⑥H+前面的配平系数为6.
| A、①③⑤⑥ | B、①②④⑤ |
| C、①②③④ | D、只有①③⑥ |
用3g块状大理石与30mL 3mol/L盐酸反应制取CO2气体,若要增大反应速率,可采取的措施是( )
①改用60mL 3mol/L盐酸 ②改用30mL 6mol/L盐酸 ③改用3g粉末状大理石 ④适当升高温度.
①改用60mL 3mol/L盐酸 ②改用30mL 6mol/L盐酸 ③改用3g粉末状大理石 ④适当升高温度.
| A、①②④ | B、②③④ |
| C、①③④ | D、①②③④ |
下列各组分子中,都属于含极性键的非极性分子的是( )
| A、CO2 H2S |
| B、C2H4 CH4 |
| C、C60 C2H4 |
| D、NH3 HCl |
甲醇燃料电池的电池反应为:2CH3OH+3O2
2CO32-+6H2O,则下列说法不正确的是( )
| 放电 |
| 充电 |
| A、充电时,电能转化为化学能 |
| B、充电时,电解质溶液中pH逐渐增大 |
| C、放电时,CH3OH参与反应的电极为负极,发生还原反应 |
| D、放电时,负极的电极反应为:CH3OH-6e-+8OH-═CO32-+6H2O |
下列有关物质的性质和应用的说法均正确的是( )
| A、氢氟酸能与二氧化硅反应,可用于刻蚀玻璃 |
| B、纯碱能与盐酸反应,可用于治疗胃酸过多 |
| C、BaCO3、BaSO4都难溶于水,均可用做钡餐 |
| D、MgO、Al2O3具有很高的熔点,均可用于制造熔融烧碱的坩埚 |