��Ŀ����
7��Ϊ�����ԴΣ�����������в���һ���������Ҵ������Ҵ����ͣ����Դ���һ�������ͣ��Ҵ�����������ȫȼ�յ��Ȼ�ѧ����ʽΪ��$\frac{1}{2}$C2H5OH��l��+$\frac{3}{2}$O2��g���TCO2��g��+$\frac{3}{2}$H2O��l����H=-683.4KJ/mol������˵����ȷ���ǣ�������| A�� | �÷�Ӧ�У�����������������ڷ�Ӧ��������� | |
| B�� | �÷�Ӧ�У����ѻ�ѧ����ų����� | |
| C�� | �Ҵ���ȼ����Ϊ683.4KJ/mol | |
| D�� | ��Ӧ$\frac{1}{2}$C2H5OH��l��+$\frac{3}{2}$O2��g���TCO2��g��+$\frac{3}{2}$H2O��g����H��-683.4KJ/mol |
���� A����Ӧ�Ƿ��ȷ�Ӧ����Ӧ��������������������������
B����Ӧ�����ж��ѻ�ѧ������������
C��ȼ������1mol��ȼ����ȫȼ�������ȶ�������ų���������
D����Ӧ��Һ̬ˮ������̬ˮʱ����Ҫ������������Ӧ�ʱ����-683.4kJ/mol��
��� �⣺A���÷�Ӧ���ʱ�С��0���Ƿ��ȷ�Ӧ����Ӧ���������������������������ʣ�A����
B����Ӧ�����ж��ѻ�ѧ����Ҫ������������B����
C��ȼ������1mol��ȼ����ȫȼ�������ȶ�������ų������������Ȼ�ѧ����ʽ�п�ȼ��Ϊ0.5mol����C����
D����Ӧ��Һ̬ˮ������̬ˮʱ����Ҫ������������Ӧ�ʱ����-683.4kJ/mol����D��ȷ��
��ѡD��
���� ���⿼���˷�Ӧ�����仯�ͻ�ѧ���ı仯��ϵ��ȼ���ȵĸ����жϣ���Ŀ�ѶȲ�����ȷ��Ӧ���������仯�Ĺ�ϵΪ���ؼ�������������ѧ�������Ӧ��������

��ϰ��ϵ�д�
 ������״Ԫ���Ծ�ϵ�д�
������״Ԫ���Ծ�ϵ�д�
�����Ŀ
5�����û�ѧ��Ӧԭ���о�±��Ԫ�ص��й����ʾ�����Ҫ���壮
��1�����й�����ˮ��������ȷ����aef����д��ţ���
a����ˮ�д������ֵ���ƽ��
b������ˮ��ͨ��SO2����Ư������ǿ
c������ˮ��ͨ��������$\frac{c��{H}^{+}��}{c��Cl{O}^{-}��}$��С
d����ˮϡ����ˮ����Һ�е���������Ũ�Ⱦ���С
e����ˮϡ����ˮ��ˮ�ĵ���ƽ��������Ӧ�����ƶ�
f������ˮ�еμ�ʯ����Һ���ȱ�����ɫ
��2�������ڹ�ҵ�����ż���㷺����;����ҵ��ͨ���ȼҵ�����������䷴Ӧ�����ӷ���ʽΪ2Cl-+2H2O $\frac{\underline{\;���\;}}{\;}$2OH-+Cl2��+H2�����ö��Ե缫���100mL����ʳ��ˮ��������������״����11.2mL���壬������Һ����ı仯ʱ��������Һ��pH=12��
��3�������£���֪25��ʱ�й�����ĵ���ƽ�ⳣ����
д��84����Һ����Ҫ�ɷ�ΪNaClO��¶���ڿ����з�����Ӧ���йػ�ѧ����ʽNaClO+CO2+H2O�THClO+NaHCO3������84����Һ����������Ũ���ᣩ���ʹ�ÿ��ܻᵼ���ж����������ӷ���ʽ�����й�ԭ��2HClO $\frac{\underline{\;����\;}}{\;}$2HCl+O2����
��4�����ú��⻯�صĵ�ҩƬ�ɿ��˷��䣮����ҩƬ��ȥ����Ƥ����������Թ����Ƶ���ɫˮ��Һ�������뼸�ε�����Һ��Ȼ�����Թ�����μ�����ˮ���۲쵽��Һ����ɫ��Ϊ��ɫ���������μ���ˮ����ɫ��Һ����Ϊ��ɫ����ɲ���ƽ��Һ��ɫ����ɫ��Ϊ��ɫ�Ļ�ѧ��Ӧ����ʽ�����ϵ����1��������д����
5Cl2+I2+6H2O��2HIO3+10HCl��
����˫��ˮ�����Թ����Ƶõ���ɫˮ��Һ��д����Ӧ�����ӷ���ʽH2O2+2I-+2H+=I2+2H2O��
��1�����й�����ˮ��������ȷ����aef����д��ţ���
a����ˮ�д������ֵ���ƽ��
b������ˮ��ͨ��SO2����Ư������ǿ
c������ˮ��ͨ��������$\frac{c��{H}^{+}��}{c��Cl{O}^{-}��}$��С
d����ˮϡ����ˮ����Һ�е���������Ũ�Ⱦ���С
e����ˮϡ����ˮ��ˮ�ĵ���ƽ��������Ӧ�����ƶ�
f������ˮ�еμ�ʯ����Һ���ȱ�����ɫ
��2�������ڹ�ҵ�����ż���㷺����;����ҵ��ͨ���ȼҵ�����������䷴Ӧ�����ӷ���ʽΪ2Cl-+2H2O $\frac{\underline{\;���\;}}{\;}$2OH-+Cl2��+H2�����ö��Ե缫���100mL����ʳ��ˮ��������������״����11.2mL���壬������Һ����ı仯ʱ��������Һ��pH=12��
��3�������£���֪25��ʱ�й�����ĵ���ƽ�ⳣ����
| ���ữѧʽ | HClO | H2CO3 |
| ����ƽ�ⳣ�� | K=4.7��10-8 | K1=4.3��10-7��K2=5.6��10-11 |
��4�����ú��⻯�صĵ�ҩƬ�ɿ��˷��䣮����ҩƬ��ȥ����Ƥ����������Թ����Ƶ���ɫˮ��Һ�������뼸�ε�����Һ��Ȼ�����Թ�����μ�����ˮ���۲쵽��Һ����ɫ��Ϊ��ɫ���������μ���ˮ����ɫ��Һ����Ϊ��ɫ����ɲ���ƽ��Һ��ɫ����ɫ��Ϊ��ɫ�Ļ�ѧ��Ӧ����ʽ�����ϵ����1��������д����
5Cl2+I2+6H2O��2HIO3+10HCl��
����˫��ˮ�����Թ����Ƶõ���ɫˮ��Һ��д����Ӧ�����ӷ���ʽH2O2+2I-+2H+=I2+2H2O��
2���Ի�����Ϊԭ��������������������к�Fe2O3��SiO2��Al2O3��MgO�ȣ�ʵ����ģ�ҵ���������Ʊ����죨Fe2O3����������ͼ��
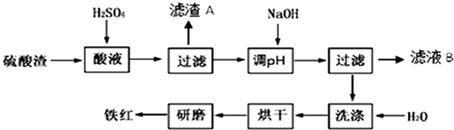
��1���������ijɷ��м�������������Ӧ����Al2O3��д�����ܹ���Fe2O3��ϡ���ᷴӦ�����ӷ�Ӧ����ʽ��Fe2O3+6H+�T2Fe3++3H2O��
��2�����������У�Ϊ��ȷ������Ĵ��ȣ�����������Ҫ������Һ��pH�ķ�Χ��3.2-3.8������������������������ʽ����ʱ��Һ��pH������
��3������A����Ҫ�ɷ�ΪSiO2����ҺB���е���Ҫ������Na2SO4��MgSO4��Al2��SO4��3��
��4�����֤��ϴ�ӻ��ڳ��ϴ��ȡ�������һ��ϴ����Һ������1��2��Ba��NO3��2��Һ���������ְ�ɫ���ǣ���ʾ��ϴ����ȫ��
��5����֪����������Ϊa kg�����������Ʊ���������Ԫ�����25%�����յõ����������Ϊb kg����ԭ������������Ԫ����������Ϊ$\frac{14b}{15a}$�����������������ݼ��㲢����������ȱ�ʾ�����

��1���������ijɷ��м�������������Ӧ����Al2O3��д�����ܹ���Fe2O3��ϡ���ᷴӦ�����ӷ�Ӧ����ʽ��Fe2O3+6H+�T2Fe3++3H2O��
��2�����������У�Ϊ��ȷ������Ĵ��ȣ�����������Ҫ������Һ��pH�ķ�Χ��3.2-3.8������������������������ʽ����ʱ��Һ��pH������
| ������ | Fe��OH��3 | Al��OH��3 | Fe��OH��2 | Mg��OH��2 |
| ��ʼ���� | 2.7 | 3.8 | 7.5 | 9.4 |
| ��ȫ���� | 3.2 | 5.2 | 9.7 | 12.4 |
��4�����֤��ϴ�ӻ��ڳ��ϴ��ȡ�������һ��ϴ����Һ������1��2��Ba��NO3��2��Һ���������ְ�ɫ���ǣ���ʾ��ϴ����ȫ��
��5����֪����������Ϊa kg�����������Ʊ���������Ԫ�����25%�����յõ����������Ϊb kg����ԭ������������Ԫ����������Ϊ$\frac{14b}{15a}$�����������������ݼ��㲢����������ȱ�ʾ�����
12������˵������ȷ���ǣ�������
| A�� | �Ҵ����Ҷ�������ͬϵ�� | |
| B�� | 1-��ϩ����˳���칹�� | |
| C�� | ����������ˮ�У���ˮ��ɫ������Ϊ�����˼ӳɷ�Ӧ | |
| D�� | ����ʽΪC3H8��C6H14�������л���һ����Ϊͬϵ�� |
19����ʯīΪ�缫��������е�����������ʵ���Ũ�ȵĻ����Һ�������������ռ������������������ȵ��ǣ�������
| A�� | ���������Ȼ��ƵĻ����Һ | B�� | ����ͭ������صĻ����Һ | ||
| C�� | Na2CO3��NaOH�����Һ | D�� | CuCl2��HCl�����Һ |
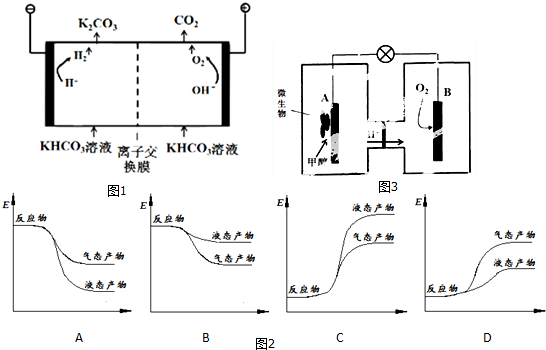
 ��D�����ʵ���������ȩ��
��D�����ʵ���������ȩ�� ��ӦFe+H2SO4�TFeSO4+H2���������仯������ͼ��ʾ��
��ӦFe+H2SO4�TFeSO4+H2���������仯������ͼ��ʾ��