题目内容
20.在室温下,下列各组微粒在溶液中能大量共存的是( )| A. | Na+、Ba2+、NO3-、Cl-、 | B. | H+、Fe2+、ClO-、SO42- | ||
| C. | K+、Fe3+、Cl-、SCN- | D. | NH4+、Al3+、SiO32-、CO32- |
分析 根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应、水解反应等,则离子大量共存,以此来解答.
解答 解:A.该组离子之间不反应,可大量共存,故A选;
B.H+、Fe2+、ClO-发生氧化还原反应,不能共存,故B不选;
C.Fe3+、SCN-结合生成络离子,不能共存,故C不选;
D.Al3+分别与SiO32-、CO32-相互促进水解,不能共存,故D不选;
故选A.
点评 本题考查离子共存,为高频考点,把握常见离子之间的反应为解答本题的关键,侧重考查复分解反应、氧化还原反应、水解反应,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
15.在pH=1的溶液中,下列离子组能大量共存且溶液为无色透明的是( )
| A. | Na+、K+、OH-、Cl- | B. | Na+、Cu2+、SO42-、NO3- | ||
| C. | Mg2+、Na+、SO42-、Cl- | D. | Ba2+、HCO3-、NO3-、K+ |
5.实验室制备Al2S3,下列方案可行的是( )
| A. | 将AlCl3溶液与Na2S溶液混合 | B. | 将H2S气体通入Al2(SO4)3溶液中 | ||
| C. | 将Al(NO3)3固体与K2S固体混合 | D. | 将金属铝与硫黄混合加热 |
4.根据下列实验操作和现象所得到的结论正确的是( )
| 选项 | 实验操作和现象 | 结论 |
| A | 含有酚酞的Na2CO3溶液中加入少量BaCl2固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| B | 用铂丝蘸取少量某溶液进行焰色反应,若火焰呈黄色 | 原溶液一定有Na+,一定无K+ |
| C | NaI溶液$\stackrel{30%H_{2}O_{2}}{→}$$\stackrel{稀硝酸及淀粉}{→}$溶液变蓝色 | 酸性条件下H2O2的氧化性比I2强 |
| D | 将乙醇与浓硫酸共热至170℃,所得气体通入酸性高锰酸钾溶液中,溶液褪色 | 说明乙醇发生消去反应生成乙烯 |
| A. | A | B. | B | C. | C | D. | D |
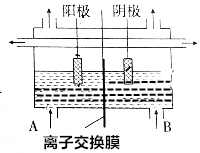 工业上电解饱和食盐水的方法之一是将两个电极室用离子交换膜隔开(如图所示),其目的是防止H2与Cl2混合发生爆炸,防止Cl2与NaOH反应生成NaClO,使NaOH不纯,阳极室(A处)加入饱和食盐水,阴极室(B极)加入水或稀氢氧化钠溶液,离子交换膜只许Na+离子通过.
工业上电解饱和食盐水的方法之一是将两个电极室用离子交换膜隔开(如图所示),其目的是防止H2与Cl2混合发生爆炸,防止Cl2与NaOH反应生成NaClO,使NaOH不纯,阳极室(A处)加入饱和食盐水,阴极室(B极)加入水或稀氢氧化钠溶液,离子交换膜只许Na+离子通过.