题目内容
根据下列化学方程式:2FeCl3+2KI=2FeCl2+2KCl+I2,2FeCl2+Cl2=2FeCl3,2KMnO4+16HCl=2MnCl2+5Cl2↑+8H2O+2KCl,判断各物质氧化性由强到弱的顺序正确是( )
| A、I2>Cl2>FeCl3>KMnO4 |
| B、KMnO4>Cl2>FeCl3>I2 |
| C、Cl2>I2>FeCl3>KMnO4 |
| D、FeCl3>KMnO4>Cl2>I2 |
考点:氧化性、还原性强弱的比较
专题:
分析:依据氧化还原反应中,氧化剂的氧化性大于氧化产物分析判断,依据各步反应,标注元素化合价变化,判断氧化剂、氧化产物.
解答:
解:2FeCl3+2KI=2FeCl2+2KCl+I2中,FeCl3是氧化剂,氧化KI为I2,氧化性FeCl3>I2;
2FeCl2+Cl2=2FeCl3反应中Cl2是氧化剂,氧化FeCl2得到氧化产物FeCl3,氧化性Cl2>FeCl3;
2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O反应中KMnO4做氧化剂,氧化HCl得到氧化产物Cl2,氧化性KMnO4>Cl2;
综上所述氧化性由大到小的顺序为:KMnO4>Cl2>FeCl3>I2,
故选B.
2FeCl2+Cl2=2FeCl3反应中Cl2是氧化剂,氧化FeCl2得到氧化产物FeCl3,氧化性Cl2>FeCl3;
2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O反应中KMnO4做氧化剂,氧化HCl得到氧化产物Cl2,氧化性KMnO4>Cl2;
综上所述氧化性由大到小的顺序为:KMnO4>Cl2>FeCl3>I2,
故选B.
点评:本题考查了氧化还原反应的强弱规律分析判断,注意元素化合价变化判断氧化剂和氧化产物,依据规律氧化剂氧化性大于氧化产物分析判断得到顺序,题目较简单.

练习册系列答案
相关题目
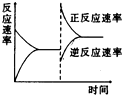 如图是改变某一外界条件后反应A2(s)+3B2(g)?2C(g)△H<0的反应速率与时间图象,则改变的条件可能是( )
如图是改变某一外界条件后反应A2(s)+3B2(g)?2C(g)△H<0的反应速率与时间图象,则改变的条件可能是( )| A、升高温度,同时加压 |
| B、保持体系压强不变加入反应物A2 |
| C、降低温度,同时减压 |
| D、保持体系压强不变加入反应物B2 |
有下列物质:①白磷;②金刚石;③石墨;④二氧化硅;⑤甲烷;⑥四氯化碳;⑦单质硅;⑧铵根离子.其分子结构或晶体结构单元中存在正四面体的是( )
| A、除③外 | B、①②⑤⑥ |
| C、除③⑧外 | D、除③④⑦⑧ |
锑(Sb)在自然界中一般以硫化物的形式存在,我国锑的蕴藏量占世界第一.从硫化物中提取单质锑一般先在高温下将硫化物转化为氧化物,再用碳还原:关于反应①、②的说法正确的是( )
①2Sb2S3+3O2+6Fe
Sb4O6+6FeS,
②Sb4O6+6C
4Sb+6CO↑.
①2Sb2S3+3O2+6Fe
| ||
②Sb4O6+6C
| ||
| A、反应①、②中的氧化剂分别是Sb2S3、Sb4O6 |
| B、反应①中每生成3molFeS时,共转移6 mol电子 |
| C、反应②说明高温下Sb的还原性比C强 |
| D、每生成4 molSb时,反应①与反应②中还原剂的物质的量之比为2:1 |
如图表示1~18号元素原子的结构或性质随核电荷数递增的变化.图中纵坐标表示( )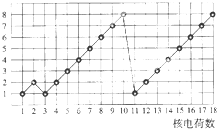

| A、最外层电子数 | B、原子半径 |
| C、最高化合价 | D、电子层数 |
发现了电子,并提出了“葡萄干面包式”的原子模型的科学家是( )
| A、玻尔 | B、道尔顿 |
| C、汤姆生 | D、卢瑟福 |
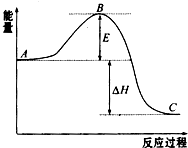 2SO2(g)+O2 (g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1
2SO2(g)+O2 (g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1