题目内容
14.下列表示正确的是( )| A. | Cl-离子的结构示意图: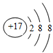 | B. | 乙炔的结构式:CH≡CH | ||
| C. | CH4的球棍模型: | D. | CO2的电子式: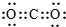 |
分析 A.氯离子的核电荷数为17,最外层达到8电子稳定结构;
B.结构式中需要用短线代替所有的共用电子对;
C. 为甲烷的比例模型,不是球棍模型;
为甲烷的比例模型,不是球棍模型;
D.二氧化碳分子中含有两个碳碳双键,氧原子最外层满足8电子稳定结构.
解答 解:A.Cl-离子核外电子总数为18,其离子结构示意图为: ,故A正确;
,故A正确;
B.乙炔分子中含有1个碳碳三键,其正确的结构式为:H-C≡C-H,故B错误;
C.甲烷分子为正四面体结构,碳原子的相对体积大于氢原子,甲烷的球棍模型为: ,故C错误;
,故C错误;
D.CO2是共价化合物,其结构式为O=C=O,碳原子和氧原子之间有2对电子,其电子式为 ,故D错误;
,故D错误;
故选A.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及电子式、比例模型与球棍模型、离子结构示意图、结构式等知识,明确常见化学用语的概念及书写原则为解答关键,试题有利于培养学生的分析能力及规范答题能力.

练习册系列答案
相关题目
4.某溶液仅含 Fe2+?Na+?Al3+?Ba2+?SO42-?NO3-?Cl-中的4种离子,所含离子的物质的量均为1mol,若向该溶液中加入过量的稀硫酸,有气体产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)?下列说法不正确的是
( )
( )
| A. | 该溶液中所含的离子是:Fe2+?Na+?SO42-?NO3-? | |
| B. | 若向该溶液中加入过量的稀硫酸,产生的气体在空气中能变成红棕色 | |
| C. | 若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液显血红色 | |
| D. | 若向该溶液中加入足量的NaOH 溶液,充分反应后,过滤?洗涤?灼烧,最终所得固体的质量为72g |
5.元素的性质随着元素原子序数的递增而呈周期性变化的根本原因是( )
| A. | 元素原子的核外电子排布呈周期性变化 | |
| B. | 元素的原子序数呈周期性变化 | |
| C. | 元素的化合价呈周期性变化 | |
| D. | 元素的金属性、非金属性呈周期性变化 |
2.下列叙述正确的是( )
| A. | 硫酸的氢离子浓度大于盐酸 | |
| B. | pH值越大,酸性越强 | |
| C. | pH=7的溶液一定呈中性 | |
| D. | 酸性溶液中氢离子浓度一定大于氢氧根离子浓度 |
9.下列说法错误的是( )
| A. | 石油中含有C5~C11的烷烃,可以通过石油的分馏得到汽油 | |
| B. | 含C18以上烷烃的重油经过催化裂化可以得到汽油 | |
| C. | 石油裂解是为了获得更多化工原料,如乙烯、丙烯等 | |
| D. | 石油分馏出来的各馏分是纯净物 |
19.火法炼铜首先要焙烧黄铜矿(主要成分为CuFeS2,其中Cu、Fe均为+2价),其反应为:2CuFeS2+O2 $\frac{\underline{\;高温\;}}{\;}$Cu2S+2FeS+SO2关于此反应,下列说法不正确的是( )
| A. | CuFeS2中被氧化和被还原的原子数之比为2:1 | |
| B. | 该反应中有两种物质作氧化剂 | |
| C. | 每生成1mol SO2,反应中转移6mol电子 | |
| D. | C uFeS2中只有硫元素被氧化 |
6.下列属于共价化合物的是( )
| A. | KF | B. | MgO | C. | H2SO4 | D. | HD |
4.下列物质中不属于合金的是( )
| A. | 不锈钢 | B. | 硬铝 | C. | 生铁 | D. | 水银 |

 +NaHCO3→
+NaHCO3→ +H2O+CO2↑;
+H2O+CO2↑;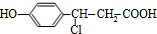 +3NaOH$→_{△}^{H_{2}O}$
+3NaOH$→_{△}^{H_{2}O}$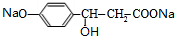 +NaCl+2H2O.
+NaCl+2H2O.