题目内容
4.杀鼠灵是一种抗凝血性杀毒剂,其结构简式如图,下列说法正确的是( )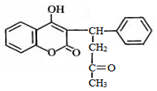
| A. | 分子中有1个手性碳原子 | B. | 遇FeCl3溶液显紫色 | ||
| C. | 1mol杀鼠灵最多能与9molH2反应 | D. | 能发生加成、取代、氧化反应 |
分析 由结构可知,与右侧苯环相连的C连接4个不同基团,分子中含碳碳双键、-OH、-COOC-、羰基,结合烯烃、醇、酯、酮的性质来解答.
解答 解:A.只有与右侧苯环相连的C连接4个不同基团,则分子中有1个手性碳原子,故A正确;
B.不含酚-OH,不能遇FeCl3溶液显紫色,故B错误;
C.只有2个苯环、1个碳碳双键、1个羰基与氢气发生加成反应,则1mol杀鼠灵最多能与8molH2反应,故C错误;
D.含碳碳双键可发生加成、氧化反应,含-OH可发生取代、氧化反应,故D正确;
故选AD.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意烯烃、酯的性质及-COOC-不能加成,题目难度不大.

练习册系列答案
相关题目
19.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 使甲基橙变红的溶液:Na+、NH4+、SO32-、Cl- | |
| B. | $\frac{{K}_{W}}{c({H}^{+})}$=0.1mol/L的溶液:K+、Na+、SiO32-、CO32- | |
| C. | SO2的饱和溶液:Na+、K+、ClO-、SO42- | |
| D. | 由水电离产生的c(H+)=1×10-12 mol•L-1的溶液:Fe3+、K+、NO3-、SO42- |
20.短周期元素A、B、C、D,其简单离子aA2+、bB+、cC3+、dD-具有相同的电子层结构下列说法中正确的是( )
| A. | 原子序数:b>a>c>d | B. | 最外层电子数:D>C>A>B | ||
| C. | 离子半径:C3+>D->B+>A2+ | D. | 单质的还原性:A>B>C>D |
12.下列有关说法正确的是( )
| A. | 酸和碱发生反应一定只生成盐和水 | |
| B. | 根据溶液酸性强弱,将酸分成强酸和弱酸 | |
| C. | 利用丁达尔效应,可以鉴别溶液和胶体 | |
| D. | 铝的单质和氧化物,与所有酸和碱均能发生化学反应 |
19.I.有些食品包装袋中会有一个小纸袋,上面写着“干燥剂”,其主要成分是生 石灰(CaO)
(1)生石灰所属的物质类型①②④(用序号填空).
①金属氧化物 ②碱性氧化物 ③碱 ④碱性干燥剂
(2)生石灰可做干燥剂的理由是CaO+H2O═Ca(OH)2(用化学方程式表示)
(3)硅胶(主要成分是二氧化硅)也是一种很好的干燥剂.用硅胶比用生石灰作 干燥剂的优点是①②(用序号填空).
①腐蚀性低 ②使用时间长
II.图是某儿童微量元素体检报告单的部分数据:
某医疗机构临床检验结果报告单
根据表的数据,回答下列问题:
(1)该儿童铁(或Fe) 元素含量偏低
(2)报告单中“μmol/L”是浓度 (填“质量”、“体积”或“浓度”) 的单位
(3)服用维生素C可使食物中的Fe3+转化为Fe2+.在这个过程中体现维生素C的还原性 (填“氧化性”或“还原性”)
(4)缺铁性贫血患者应补充Fe2+.一些补铁剂以硫酸亚铁为主要成分,用硫酸亚铁制成药片时外表包有一层特殊的糖衣,推测糖衣的作用是防止Fe2+被氧化.
(1)生石灰所属的物质类型①②④(用序号填空).
①金属氧化物 ②碱性氧化物 ③碱 ④碱性干燥剂
(2)生石灰可做干燥剂的理由是CaO+H2O═Ca(OH)2(用化学方程式表示)
(3)硅胶(主要成分是二氧化硅)也是一种很好的干燥剂.用硅胶比用生石灰作 干燥剂的优点是①②(用序号填空).
①腐蚀性低 ②使用时间长
II.图是某儿童微量元素体检报告单的部分数据:
某医疗机构临床检验结果报告单
| 某医疗机构临床检验结果报告单 | ||||
| 分析项目 | 检测结果 | 单位 | 参考范围 | |
| 1 | 锌(Zn) | 115.92 | μmol/L | 66-120 |
| 2 | 铁(Fe) | 6.95↓ | mmol/L | 7.52-11.82 |
| 3 | 钙(Ca) | 1.68 | mmol/L | 1.55-2.10 |
| … | ||||
(1)该儿童铁(或Fe) 元素含量偏低
(2)报告单中“μmol/L”是浓度 (填“质量”、“体积”或“浓度”) 的单位
(3)服用维生素C可使食物中的Fe3+转化为Fe2+.在这个过程中体现维生素C的还原性 (填“氧化性”或“还原性”)
(4)缺铁性贫血患者应补充Fe2+.一些补铁剂以硫酸亚铁为主要成分,用硫酸亚铁制成药片时外表包有一层特殊的糖衣,推测糖衣的作用是防止Fe2+被氧化.
9.下列各组离子在强酸性溶液中能大量共存的是( )
| A. | K+、Na+、HCO3-、SO42- | B. | Na+、Fe3+、I-、CI- | ||
| C. | Na+、NH4+、NO3-、CI- | D. | Na+、Ba2+、SO42-、NO3- |
16.下列说法正确的是( )
| A. | 用直接加热并蒸干FeCl3溶液的方法可制得纯净的无水FeCl3 | |
| B. | 等物质的量浓度的Na2CO3溶液和CH3COONa溶液的pH,前者大于后者 | |
| C. | 中和等体积、等物质的量浓度的盐酸和醋酸溶液,消耗NaOH的物质的量不相等 | |
| D. | 对于有气体参加的反应,增大气体反应物浓度,活化分子百分数增大,反应速率加快 |
13.常温下,加水稀释10mL 0.1mol•L-1CH3COOH溶液的过程中,下列数值中始终保持增大趋势的是( )
| A. | c(H+) | B. | Ka | ||
| C. | c(OH-) | D. | $\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$ |
14.下列实验操作能达到实验目的是( )
| 实验目的 | 实验操作 | |
| A | 制备Fe(OH)3胶体 | 将NaOH溶液滴加到饱和的FeCl3溶液中 |
| B | 除去氯化铵固体中的碘单质 | 加热固体,使碘升华 |
| C | 比较S和Si非金属性强弱 | 向硅酸钠溶液中通入SO2出现浑浊 |
| D | 检验氨气是否收集满 | 用湿润的红色石蕊试纸放入试管口,试纸变蓝 |
| A. | A | B. | B | C. | C | D. | D |