题目内容
10.在实验室中,常用 KMnO4代替 MnO2与浓盐酸反应制取氯气,其反应的化学方程式为2KMnO4+16HCl(浓)=2MnCl2+5Cl2↑+2KCl+8H2O,下列叙述中正确的是( )| A. | 反应中 KMnO4被氧化 | |
| B. | 氧化产物与还原产物的物质的量之比为 2:5 | |
| C. | 每生成 1 mol Cl2时,反应中转移的电子为 2 mol | |
| D. | 每消耗 16 molHCl 时,其中作氧化剂的 HCl 是 10 mol |
分析 2KMnO4+16HCl(浓)=2MnCl2+5Cl2↑+2KCl+8H2O中,Mn元素的化合价降低,Cl元素的化合价升高,以此来解答.
解答 解:A.Mn元素的化合价降低,得到电子KMnO4被还原,故A错误;
B.氧化产物为Cl2,还原产物为MnCl2,由反应可知氧化产物与还原产物的物质的量之比为5:2,故B错误;
C.每生成1 mol Cl2时,反应中转移的电子为1mol×2×[0-(-1)]=2 mol,故C正确;
D.每消耗16 mol HCl时,由反应可知,只有10molCl失去电子,则其中做还原剂的HCl是10 mol,故D错误;
故选C.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化是解答本题的关键,侧重氧化还原反应基本概念及转移电子的考查,题目难度不大.

练习册系列答案
相关题目
20.下列反应中,不属于四种基本反应类型,但属于氧化还原反应的是( )
| A. | 2Na+2H2O═2NaOH+H2↑ | B. | CaCO3+2HCl═CaCl2+H2O+CO2↑ | ||
| C. | 2KClO3$\frac{\underline{\;\;△\;\;}}{\;}$2KCl+3O2↑ | D. | CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O |
1.对于热爱化学的你这是一道送分题.在下列给定条件的溶液中,一定能大量共存的离子组是( )
| A. | KNO3溶液:Fe2+、I-、SO42-、H+ | |
| B. | 含大量Al3+的溶液中:Cu2+、Na+、SO42-、NO3- | |
| C. | 由水电离出的c(H+)=1.0×10-12的溶液中:Ba2+、K+、Cl-、HCO3- | |
| D. | 使甲基橙呈红色的溶液:Na+、K+、SiO32-、NO3- |
18.下列说法正确的是( )
| A. | 凡是能量达到活化能的分子发生的碰撞均为有效碰撞 | |
| B. | 熵增大的反应都是自发反应,熵减少的反应都不能进行 | |
| C. | 升高温度,可逆反应的正反应速率和逆反应速率都一定增大 | |
| D. | 使用催化剂可以增加反应物分子的能量,从而增大反应速率 |
5.设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 0.5 mol Al与足量盐酸反应转移电子数为NA | |
| B. | 标准状况下,22.4 L氨气与22.4 L氮气所含原子数均为2 NA | |
| C. | 7.8gNa2O2所含的离子数为0.3NA | |
| D. | 11.2LCl2完全溶于NaOH溶液,电子转移数为0.5 NA |
15.如图烧杯中盛有海水,铁在其中被腐蚀由快到慢的顺序为( )
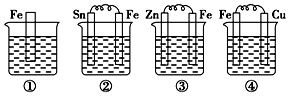

| A. | ②①③④ | B. | ④③②① | C. | ④②①③ | D. | ③②④① |
2.下列物质中属于电解质的是( )
| A. | 酒精 | B. | 氨水 | C. | 熔融的氯化钠 | D. | 铁 |
19.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 使甲基橙变红的溶液:Na+、NH4+、SO32-、Cl- | |
| B. | $\frac{{K}_{W}}{c({H}^{+})}$=0.1mol/L的溶液:K+、Na+、SiO32-、CO32- | |
| C. | SO2的饱和溶液:Na+、K+、ClO-、SO42- | |
| D. | 由水电离产生的c(H+)=1×10-12 mol•L-1的溶液:Fe3+、K+、NO3-、SO42- |
20.短周期元素A、B、C、D,其简单离子aA2+、bB+、cC3+、dD-具有相同的电子层结构下列说法中正确的是( )
| A. | 原子序数:b>a>c>d | B. | 最外层电子数:D>C>A>B | ||
| C. | 离子半径:C3+>D->B+>A2+ | D. | 单质的还原性:A>B>C>D |