题目内容
10.N与H形成的化合物肼(N2H4)可用作火箭燃料,燃烧时发生的反应是:2N2H4(l)+N2O4(l)═3N2(g)+4H2O(g)△H=-1038.7kJ/mol.若该反应中有4mol N-H键断裂,则形成的π键有3mol.分析 反应中有4mol N-H键断裂,则参加反应的N2H4为1mol,根据方程式计算生成N2的物质的量,氮气分子结构式为N≡N,三键中含有1个σ键、2个π键.
解答 解:反应中有4mol N-H键断裂,则参加反应的N2H4为1mol,根据2N2H4(l)+N2O4(l)═3N2(g)+4H2O(g)可知生成N2的物质的量为1mol×$\frac{3}{2}$=1.5mol,氮气分子结构式为N≡N,三键中含有1个σ键、2个π键,故形成的π键为1.5mol×2=3mol,
故答案为:3.
点评 本题考查化学方程式计算、化学键,比较基础,明确分子结构即可解答.

练习册系列答案
相关题目
6.常温下,将10mL0.1mol•L-1的醋酸溶液稀释到100mL,稀释过程中,下列数值逐渐减小的是( )
| A. | c(H+)•c(OH-) | B. | $\frac{c{({CH}_{3}COO}^{-})•c{(H}^{+})}{c({CH}_{3}COOH)}$ | ||
| C. | $\frac{c{(H}^{+})}{c({CH}_{3}COOH)}$ | D. | $\frac{c({CH}_{3}C{OO}^{-})}{c{(OH}^{-})}$ |
15.金属钛易于和肌肉长在一起,可用于制造各种人造关节,因此被称为“生物金属”.工业上由钛铁矿(主要成分为FeTiO3,含少量Fe2O3)制备钛的工艺流程如下:
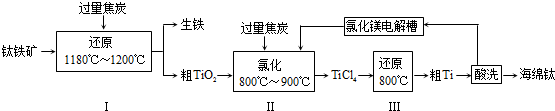
(1)进行步骤Ⅰ前,钛铁矿需要先粉碎成细颗粒,目的为增大反应速率.
(2)步骤Ⅰ中所发生的主要反应的化学方程式为FeTiO3+C$\frac{\underline{\;1180℃-1200℃\;}}{\;}$Fe+TiO2+CO↑.
(3)将步骤Ⅱ中所发生的主要反应记为反应①,则①的化学方程式为TiO2+2Cl2+2C$\frac{\underline{\;高温\;}}{\;}$TiCl4+2CO;有同学认为步骤Ⅱ中的物质转化中只需通入氯气,而无需加入焦炭就能实现,即发生反应②:TiO2+2Cl2 $\frac{\underline{\;高温\;}}{\;}$ TiCl4+O2.已知相关数据如下:
结合上表数据,从反应进行的方向角度分析加入焦炭的必要性加入焦炭后发生反应①,与反应②相比,△H减小,△S增大,更有利于反应在较低温度下向右进行.
(4)步骤Ⅲ中,反应物TiCl4应避免接触水,原因为防止TiCl4水解;反应结束后,用盐酸洗涤粗Ti,除去Mg、MgCl2(填化学式),即可制得海绵钛.

(1)进行步骤Ⅰ前,钛铁矿需要先粉碎成细颗粒,目的为增大反应速率.
(2)步骤Ⅰ中所发生的主要反应的化学方程式为FeTiO3+C$\frac{\underline{\;1180℃-1200℃\;}}{\;}$Fe+TiO2+CO↑.
(3)将步骤Ⅱ中所发生的主要反应记为反应①,则①的化学方程式为TiO2+2Cl2+2C$\frac{\underline{\;高温\;}}{\;}$TiCl4+2CO;有同学认为步骤Ⅱ中的物质转化中只需通入氯气,而无需加入焦炭就能实现,即发生反应②:TiO2+2Cl2 $\frac{\underline{\;高温\;}}{\;}$ TiCl4+O2.已知相关数据如下:
| 反应 | △H/kJ•mol-1 | △S/J•K-1•mol-1 |
| ① | -72.1 | +220 |
| ② | +149 | +41 |
(4)步骤Ⅲ中,反应物TiCl4应避免接触水,原因为防止TiCl4水解;反应结束后,用盐酸洗涤粗Ti,除去Mg、MgCl2(填化学式),即可制得海绵钛.
2.已知:H2O(g)═H2O(l)△H=Q1KJ•mol-1
C2H5OH(g)═C2H5OH(l)△H=Q2KJ•mol-1
C2H5OH(g)+3O2(g)═2CO2(g)+3H2O(g)△H=Q3KJ•mol-1
则反应C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(l)△H=( ) KJ•mol-1.
C2H5OH(g)═C2H5OH(l)△H=Q2KJ•mol-1
C2H5OH(g)+3O2(g)═2CO2(g)+3H2O(g)△H=Q3KJ•mol-1
则反应C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(l)△H=( ) KJ•mol-1.
| A. | Q3-Q2+3 Q1 | B. | Q3+Q2+Q1 | C. | 3Q3-Q2+Q1 | D. | Q2-Q3+3 Q1 |
19.同温同压下,1体积X2气体与3体积Y2气体化合生成2体积气体化合物Z,则化合物Z的化学式可表示为( )
| A. | XY3 | B. | XY | C. | X3Y | D. | X2Y3 |
20.溴酸银(AgBrO3)溶解度随温度变化曲线如图所示,下列说法错误的是( )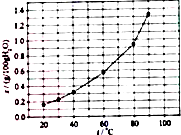

| A. | 溴酸银的溶解是吸热过程 | |
| B. | 温度升高时溴酸银溶解速度加快 | |
| C. | 60℃时溴酸银的Ksp约等于6×10-3 | |
| D. | 若硝酸钾中含有少量溴酸银,可用它们的溶解度随温度变化的差异进行分离 |
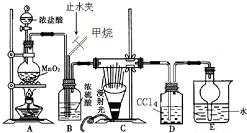 利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实.某化学兴趣小组拟在实验室中模拟上述过程,其设计的模拟装置如图:
利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实.某化学兴趣小组拟在实验室中模拟上述过程,其设计的模拟装置如图: B.
B. C.
C.