题目内容
17.偏二甲肼( )是运载火箭的主体燃料.C2H8N2物质中含碳碳单键的同分异构体共有( )
)是运载火箭的主体燃料.C2H8N2物质中含碳碳单键的同分异构体共有( )| A. | 2种 | B. | 3 种 | C. | 4种 | D. | 5种 |
分析 根据化学键连接方式,列出C2H8N2可能有的结构,据此判断.
解答 解:根据化学键连接方式,C2H8N2可能有6种结构:
CH3NH-NHCH3、CH3CH2NHNH2、(CH3)2N-NH2、NH2CH2CH2NH2、CH3CH(NH2)2、CH3NHCH2NH2,其中含碳碳单键的同分异构体为CH3CH2NHNH2、NH2CH2CH2NH2,CH3CH(NH2)2共3种,故选B.
点评 本题考查根据分子式书写同分异构体的知识,难度中等,关键根据化学键连接方式,列出C2H8N2可能有的结构.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8.利用如图所示装置进行下列实验,能得出相应实验结论的是( )
| 选项 | ① | ② | ③ | 实验结论 |  |
| A | 浓盐酸 | MnO2 | NaBr溶液 | 氧化性Cl2>Br2 | |
| B | 浓氨水 | 碱石灰 | AgNO3溶液 | AgOH具有两性 | |
| C | 浓硫酸 | Na2SO3 | FeCl3溶液 | SO2具有还原性 | |
| D | 稀盐酸 | Na2CO3 | Na2SiO3溶液 | 非金属性:Cl>C>Si |
| A. | A | B. | B | C. | C | D. | D |
5.已知25℃时有关弱酸的电离平衡常数如下表:
下列关于Na2CO3溶液说法不正确的是( )
| 弱酸化学式 | HCN | H2CO3 |
| 电离平衡常数(25℃) | 4.9×10-10 | K1=4.3×10-7K2=5.6×10-11 |
| A. | Na2CO3溶液中滴入等体积、等浓度的盐酸后,溶液中一定存在:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(Cl-)+c(OH-) | |
| B. | Na2CO3溶液中通一定量的CO2气体后,溶液中一定存在:c(Na+)=c(H2CO3)+c(HCO3-)+c(CO32-) | |
| C. | Na2CO3溶液加水稀释后,c(H+)增大 | |
| D. | Na2CO3溶液中加入过量HCN,反应方程式为:Na2CO3+HCN=NaHCO3+NaCN |
12.短周期元素A、B、C、D的原子序数逐渐增大,A、B的最高正价与最低负价之和都为0,D与A同主族,C的一种单质具有杀菌的作用,少量能使人精神振奋,E的合金是目前使用比较广泛的合金,下列说法正确的是( )
| A. | 简单离子的半径:r(A)<r(C)<r(D)<r(E) | |
| B. | 元素B的最简单气态氧化物的稳定性比C的强 | |
| C. | D2C2与A2C2的漂白原理相同 | |
| D. | 元素E的氧化物能溶于B或D的最高价氧化物对应的水化物中 |
2.化学与生活密切相关,下列说法不正确的是( )
| A. | Na2O2可用作供氧剂 | |
| B. | 硅胶多孔,吸水能力强,常用作袋装食品的干燥剂 | |
| C. | SO2具有漂白性,常用药食品的漂白 | |
| D. | K2FeO4可用于水的净化 |
9.最近,科学家在甲烷的低温活化与二氧化碳加氢制取乙酸的研究上取得了突破,其反应原理如下:CH4$→_{-H_{2}}^{催化剂}$CHX$→_{H_{2}}^{CO_{2}}$CH3COOH,下列说法错误的是( )
| A. | CO2、CH3COOH均为共价化合物 | |
| B. | 每生成1molCH3COOH,要消耗22.4LCO2 | |
| C. | CO2、CH3COOH分子中均含σ键和π键 | |
| D. | CH4$→_{-H_{2}}^{催化剂}$CHX属于氧化反应 |
7.用下列装置完成相关实验,不合理的是( )
| A. | 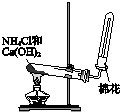 用a制备并收集氨气 | B. | 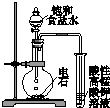 用b制备并检验乙炔 | ||
| C. | 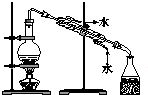 用c蒸馏海水得到淡水 | D. | 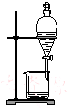 用d分离Na2CO3溶液与CH3COOC2H5 |