题目内容
下列各组离子能大量共存,向溶液中通入足量相应气体后,各离子还能大量存在的是( )
| A、氯气:K+、Ba2+、SiO32-、NO3- |
| B、二氧化硫:Na+、NH4+、SO32-、C1- |
| C、氨气:K+、Na+、AlO2-、CO32- |
| D、甲醛:Ca2+、Mg2+、MnO4-、NO3- |
考点:离子共存问题
专题:离子反应专题
分析:根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应等,则离子大量共存,以此来解答.
解答:
解:A.Ba2+、SiO32-结合生成沉淀,不能大量共存,故A错误;
B.该组离子之间不反应,可大量共存,但通入二氧化硫与SO32-反应,不能大量共存,故B错误;
C.该组离子之间不反应,可大量共存,通入氨气扔不反应,不能大量共存,故C正确;
D.甲醛与MnO4-发生氧化还原反应,不能大量共存,故D错误;
故选C.
B.该组离子之间不反应,可大量共存,但通入二氧化硫与SO32-反应,不能大量共存,故B错误;
C.该组离子之间不反应,可大量共存,通入氨气扔不反应,不能大量共存,故C正确;
D.甲醛与MnO4-发生氧化还原反应,不能大量共存,故D错误;
故选C.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
对于以下反应:改变反应物用量时,不能用同一个离子方程式表示的是( )
①KHCO3溶液与石灰水反应
②Na2SO3溶液与稀盐酸反应
③Si与烧碱溶液反应
④Fe与稀硝酸反应.
①KHCO3溶液与石灰水反应
②Na2SO3溶液与稀盐酸反应
③Si与烧碱溶液反应
④Fe与稀硝酸反应.
| A、①②③ | B、①②④ |
| C、①③④ | D、②③④ |
美国海军航空站安装了MCFC型燃料电池,该电池可同时供应电和水蒸气,其工作温度为600℃~700℃,所用燃料为H2,电解质为熔融的K2CO3,已知该电池的总反应为2H2+O2═2H2O,负极反应为H2+CO32--2e-═H2O+CO2,则下列推断正确的是( )
| A、正极反应为:4OH-═O2+2H2O+4e- |
| B、放电时CO32- 向负极移动 |
| C、电池供应1mol水蒸气,转移的电子数为4mol |
| D、放电时CO32- 向正极移动 |
在甲、乙两烧杯溶液中,共含有大量的Cu2+、K+、H+、NO3-、CO32-、OH-.已知甲烧杯的溶液呈蓝色,则乙烧杯中大量存在的离子是( )
| A、Cu2+、H+、NO3- |
| B、K+、CO32-、OH- |
| C、CO32-、OH-、NO3- |
| D、K+、H+、NO3- |
氢气是人类最理想的能源.已知在25℃、101kPa下,1g氢气完全燃烧生成液态水时放出热量142.9kJ,今有如下三个热化学方程式下列关于它们的表述正确的是?( )
(1)H2(g)+
O2(g)=H2O(g)△H1=a kJ?mol-1??
(2)H2O(l)=H2(g)+
O2(g)△H2=b kJ?mol-1??
(3)2H2(g)+O2(g)=2H2O(l)△H3=c kJ?mol-1??
(1)H2(g)+
| 1 |
| 2 |
(2)H2O(l)=H2(g)+
| 1 |
| 2 |
(3)2H2(g)+O2(g)=2H2O(l)△H3=c kJ?mol-1??
| A、2b=c |
| B、b=285.8? |
| C、a=-b? |
| D、氢气的燃烧热为a kJ?mol-1 |
下列说法正确的是( )
| A、将NaOH和氨水溶液各稀释一倍,两者的OH-浓度均减少到原来的一半 |
| B、如果盐酸的浓度是醋酸浓度的二倍,则盐酸中的H+浓度是醋酸中的H+浓度的二倍多 |
| C、中和等体积、等物质的量浓度的盐酸和醋酸溶液,盐酸所需氢氧化钠多于醋酸 |
| D、物质的量相同的NaClO溶液和HClO溶液中所含ClO-的量相同 |
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )
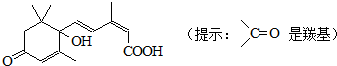
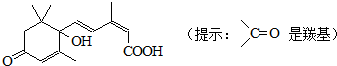
| A、含有羟基、羰基、羧基、酯基 |
| B、含有苯环、羟基、羰基、羧基 |
| C、含有碳碳双键、羟基、羰基、羧基 |
| D、含有碳碳双键、苯环、羟基、羰基 |
