题目内容
在甲、乙两烧杯溶液中,共含有大量的Cu2+、K+、H+、NO3-、CO32-、OH-.已知甲烧杯的溶液呈蓝色,则乙烧杯中大量存在的离子是( )
| A、Cu2+、H+、NO3- |
| B、K+、CO32-、OH- |
| C、CO32-、OH-、NO3- |
| D、K+、H+、NO3- |
考点:离子共存问题
专题:
分析:甲烧杯的溶液呈蓝色,则含有Cu2+,根据离子共存可知,甲中不存在CO32-、OH-离子,CO32-、OH-应该存在于乙烧杯中,乙烧杯的阳离子不可能为H+,只能为K+,据此进行解答.
解答:
解:甲烧杯的溶液呈蓝色说明甲中含有Cu2+,而CO32-、OH-离子不能与Cu2+离子大量共存,故CO32-、OH-只能存在于乙烧杯中,
乙烧杯中含有CO32-、OH-离子,由于H+离子与CO32-、OH-离子反应,则H+离子只能存在于甲烧杯中,
根据溶液的电中性,甲中还应含有NO3-,乙中还应含有K+,
故甲中含有的离子为:Cu2+、H+、NO3-,乙中含有的离子为:K+、OH-、CO32-,
故选B.
乙烧杯中含有CO32-、OH-离子,由于H+离子与CO32-、OH-离子反应,则H+离子只能存在于甲烧杯中,
根据溶液的电中性,甲中还应含有NO3-,乙中还应含有K+,
故甲中含有的离子为:Cu2+、H+、NO3-,乙中含有的离子为:K+、OH-、CO32-,
故选B.
点评:本题考查离子共存的判断,为高考中的高频题,题目难度中等,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;试题试题侧重对学生基础知识的训练和检验,有利于提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
在蒸馏实验中,下列叙述不正确的是( )
A、在蒸馏烧瓶中盛约
| ||
| B、收集蒸馏水时,应弃去开始馏出的部分 | ||
| C、冷水从冷凝管下口入,上口出 | ||
| D、将温度计水银球插入自来水中 |
下列各组离子能大量共存,向溶液中通入足量相应气体后,各离子还能大量存在的是( )
| A、氯气:K+、Ba2+、SiO32-、NO3- |
| B、二氧化硫:Na+、NH4+、SO32-、C1- |
| C、氨气:K+、Na+、AlO2-、CO32- |
| D、甲醛:Ca2+、Mg2+、MnO4-、NO3- |
下列叙述正确的是( )
| A、强电解质一定易溶于水,弱电解质都难溶于水 |
| B、NaHCO3的热稳定性和溶解度均大于Na2CO3 |
| C、过量的铜与浓硝酸反应有一氧化氮生成 |
| D、Fe与S混合加热生成FeS2 |
下列说法正确的是( )
| A、放热反应都是自发的,吸热反应都是非自发的 |
| B、自发反应一定是熵增大,非自发反应一定是熵减少或不变 |
| C、△H<0,△S>0的反应一定是自发反应 |
| D、△H>0,△S>0的反应低温时是自发反应 |
下列物质中,属于强电解质的是( )
| A、SO3 |
| B、C2H5OH |
| C、CH3COOH |
| D、CH3COONH4 |
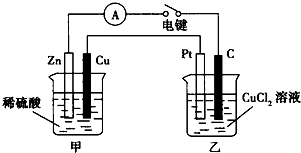 某兴趣小组的同学用如图所示装置研究有关电化学的问题.当闭合该装置的电键时,观察到电流表的指针发生了偏转.
某兴趣小组的同学用如图所示装置研究有关电化学的问题.当闭合该装置的电键时,观察到电流表的指针发生了偏转.