题目内容
18.向明矾溶液中逐滴加入Ba(OH)2溶液,当SO42-全部沉淀时,铝元素的主要存在形式为( )| A. | AlO2- | B. | Al3+ | C. | Al(OH)3 | D. | Al(OH)3和Al3+ |
分析 明矾的化学式为KAl(SO4)2•12H2O,设明矾为1mol,则溶液中含有1molAl3+,2molSO42-,根据反应:SO42-+Ba2+=BaSO4↓,Al3++4OH-=AlO2-+2H2O判断.
解答 解:明矾的化学式为KAl(SO4)2•12H2O,设明矾为1mol,则溶液中含有1molAl3+,2molSO42-,由反应SO42-+Ba2+=BaSO4↓可知,使SO42-全部转化成BaSO4沉淀,需要2molBa(OH)2,则加入4molOH-,则发生Al3++4OH-=AlO2-+2H2O,所以最后溶液中存在AlO2-,
故选A.
点评 本题考查离子方程式的书写,题目难度中等,本题中注意判断使SO42-全部转化成BaSO4沉淀需要Ba(OH)2的物质的量,根据Al3+和OH-物质的量的关系判断反应产物.

练习册系列答案
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
8.下列叙述中错误的是( )
| A. | 共价化合物中只有共价键,一定没有离子键 | |
| B. | 金属和非金属一定形成离子化合物 | |
| C. | 含有离子键的化合物一定是离子化合物 | |
| D. | 离子化合物中可能含有极性共价键 |
6.既能与酸又能与碱反应是两性化合物的特征.下列物质属于两性化合物的是( )
| A. | A1 | B. | Na2CO3 | C. | A1(OH)3 | D. | (NH4)2SO4 |
13.下有物质归类正确的是( )
| A. | 胶体:豆浆、墨水、血液、生理盐水 | |
| B. | 单质:冰、液氯、臭氧、红磷 | |
| C. | 混合物:矿泉水、84消毒液、铝热剂、四氧化三铁 | |
| D. | 常见的氧化剂:高锰酸钾、氯气、硝酸、氧气 |
3.对有关NaClO和NaCl混合溶液的叙述正确的是( )
| A. | 该溶液中,H+、NH4+、SO42-、Br-可以大量共存 | |
| B. | 该溶液中,K+、OH-、S2-、NO3-能大量共存 | |
| C. | 向该溶液中滴入少量FeSO4溶液,离子方程式为:2Fe2++ClO-+2H+→Cl-+2Fe3++H2O | |
| D. | 向该溶液中加入浓盐酸,每产生1molCl2,转移电子约为6.02×1023个 |
7.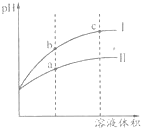 某温度下pH=2的盐酸和醋酸溶液分别加水稀释,pH值随溶液体积变化的曲线如图所示.下列说法正确的是( )
某温度下pH=2的盐酸和醋酸溶液分别加水稀释,pH值随溶液体积变化的曲线如图所示.下列说法正确的是( )
 某温度下pH=2的盐酸和醋酸溶液分别加水稀释,pH值随溶液体积变化的曲线如图所示.下列说法正确的是( )
某温度下pH=2的盐酸和醋酸溶液分别加水稀释,pH值随溶液体积变化的曲线如图所示.下列说法正确的是( )| A. | Ⅱ为盐酸稀释时pH变化曲线 | |
| B. | b点溶液的导电性比c点溶液的导电性强 | |
| C. | a点Kw数值比c点Kw数值大 | |
| D. | pH=2的盐酸和醋酸,盐酸的物质的量浓度大 |
 (1)电子表所用的某种钮扣电池的电极材料为Zn和Ag2O,电解质溶液为KOH,其电极反应式分别为Zn+2OH--2e-=ZnO+H2O Ag2O+H2O+2e-=2Ag+2OH-
(1)电子表所用的某种钮扣电池的电极材料为Zn和Ag2O,电解质溶液为KOH,其电极反应式分别为Zn+2OH--2e-=ZnO+H2O Ag2O+H2O+2e-=2Ag+2OH-